网址:http://m.1010jiajiao.com/timu3_id_78889[举报]
|
25℃时,水的电离达到平衡:H2O■H++OH-;ΔH>0,下列叙述正确的是 | |
| [ ] | |
A. |
向水中加人稀氨水,平衡逆向移动,c(OH-)降低 |
B. |
向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
C. |
向水中加人少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
D. |
将水加热,Kw增大,pH不变 |
25 ℃时,水的电离达到平衡:H2O  H++OH-;△H>0,下列叙述正确的是
(
)
H++OH-;△H>0,下列叙述正确的是
(
)
A 向水中加入氨水,平衡逆向移动,c(OH-)降低
B 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D 将水加热,KW增大,pH不变
查看习题详情和答案>>
25 ℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是 ( )
A 向水中加入氨水,平衡逆向移动,c(OH-)降低
B 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D 将水加热,KW增大,pH不变
查看习题详情和答案>>
25 ℃时,水的电离达到平衡:H2O 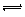 H++OH-;?△H>0,下列叙述正确的是 ( )
H++OH-;?△H>0,下列叙述正确的是 ( )
A 向水中加入氨水,平衡逆向移动,c(OH-)降低
B 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D 将水加热,KW增大,pH不变
|
25 ℃时,NH3·H2O在水中的电离达到平衡:NH3·H2O | |
| [ ] | |
A. |
向稀氨水中继续加入水,平衡正向移动, c(OH-)增大 |
B. |
向稀氨水中继续缓慢加入水, |
C. |
向稀氨水中加入少量固体 CH3COONH4,平衡逆向移动,c(H+)减小 |
D. |
将稀氨水加热 ,KW增大,pH变大 |