摘要:18.现有含杂质的试剂.科学实验中.对物质的纯度有严格的要求.只用一种试剂即可除去下列各物质中的杂质.试写出所用试剂及有关反应的离子方程式. (1)BaCl2(HCl) 选用试剂 . 离子方程式 . (2)CO2(SO2) 选用试剂 . 离子方程式 . (3)NaCl(Na2SO4) 选用试剂 . 离子方程式 . (4)FeCl2(FeCl3) 选用试剂 . 离子方程式 . (5)Na2CO3(NaHCO3) 选用试剂 . 离子方程式 . 解析:根据杂质的性质选择合适的试剂.然后根据离子反应实质进行书写.
网址:http://m.1010jiajiao.com/timu3_id_78513[举报]
近年来,湿法炼铜有了新进展,科学家发现有一种细菌在有氧气存在的酸性溶液中,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐,4CuFeS2+2H2SO4+17O2═4CuSO4+2Fe2(SO4)3+2H2O.某工厂运用该原理生产胆矾和绿矾的工艺如下:

(1)操作1的名称是______.
(2)试剂a和试剂b的化学式分别是______.
(3)简述检验某未知固体是否含有SO42-的实验过程______.
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、______并干燥.
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是______.
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
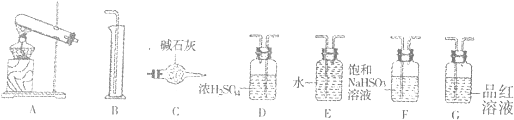
①气体的3种可能性为:______;______;有SO2、SO3和O2.
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→______→B.
查看习题详情和答案>>

(1)操作1的名称是______.
(2)试剂a和试剂b的化学式分别是______.
(3)简述检验某未知固体是否含有SO42-的实验过程______.
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、______并干燥.
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是______.
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
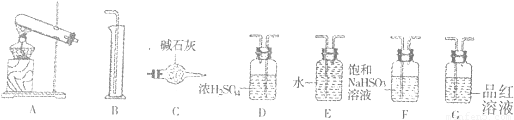
①气体的3种可能性为:______;______;有SO2、SO3和O2.
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→______→B.

近年来,湿法炼铜有了新进展,科学家发现有一种细菌在有氧气存在的酸性溶液中,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐,4CuFeS2+2H2SO4+17O2═4CuSO4+2Fe2(SO4)3+2H2O.某工厂运用该原理生产胆矾和绿矾的工艺如下:
(1)操作1的名称是______.
(2)试剂a和试剂b的化学式分别是______.
(3)简述检验某未知固体是否含有SO42-的实验过程______.
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、______并干燥.
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是______.
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
①气体的3种可能性为:______;______;有SO2、SO3和O2.
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→______→B.
查看习题详情和答案>>

(1)操作1的名称是______.
(2)试剂a和试剂b的化学式分别是______.
(3)简述检验某未知固体是否含有SO42-的实验过程______.
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、______并干燥.
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是______.
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
①气体的3种可能性为:______;______;有SO2、SO3和O2.
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→______→B.

查看习题详情和答案>>
近年来,湿法炼铜有了新进展,科学家发现有一种细菌在有氧气存在的酸性溶液中,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐,4CuFeS2+2H2SO4+17O2═4CuSO4+2Fe2(SO4)3+2H2O.某工厂运用该原理生产胆矾和绿矾的工艺如下:
(1)操作1的名称是______.
(2)试剂a和试剂b的化学式分别是______.
(3)简述检验某未知固体是否含有SO42-的实验过程______.
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、______并干燥.
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是______.
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
①气体的3种可能性为:______;______;有SO2、SO3和O2.
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→______→B.

查看习题详情和答案>>
近年来,湿法炼铜有了新进展,科学家发现有一种细菌在有氧气存在的酸性溶液中,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐,4CuFeS2+2H2SO4+17O2═4CuSO4+2Fe2(SO4)3+2H2O.某工厂运用该原理生产胆矾和绿矾的工艺如下:
(1)操作1的名称是
(2)试剂a和试剂b的化学式分别是
(3)简述检验某未知固体是否含有SO42-的实验过程
(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、
(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是
(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
①气体的3种可能性为:
②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→

查看习题详情和答案>>

(1)操作1的名称是
过滤
过滤
.(2)试剂a和试剂b的化学式分别是
硫酸、过量的铁粉
硫酸、过量的铁粉
.(3)简述检验某未知固体是否含有SO42-的实验过程
取少量的固体配制成溶液,加入盐酸无明显现象,再加入氯化钡溶液出现白色沉淀,证明含有硫酸根离子,否则没有
取少量的固体配制成溶液,加入盐酸无明显现象,再加入氯化钡溶液出现白色沉淀,证明含有硫酸根离子,否则没有
.(4)由CuSO4溶液制取纯净的CuSO4?5H2O应进行的操作是:加热浓缩、
结晶、过滤、洗涤
结晶、过滤、洗涤
并干燥.(5)在4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O反应中,被氧化的元素是
Fe和CuFeS2中的S
Fe和CuFeS2中的S
.(6)某活动小组对CuSO4分解的除CuO外的气体3种可能性进行假设,并通过实验确定气体的物质的量.
①气体的3种可能性为:
仅有SO2
仅有SO2
;仅有SO3
仅有SO3
;有SO2、SO3和O2.②为确定SO2、SO3和O2的物质的量之比,请你选用所给的仪器进行实验,按气体从左至右的方向连接各装置.顺序为:A→
D→C(→G)E或F→D→C(→G)→E
D→C(→G)E或F→D→C(→G)→E
→B.