网址:http://m.1010jiajiao.com/timu3_id_77860[举报]
某课外活动小组模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低。实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、大理石、水。试回答:
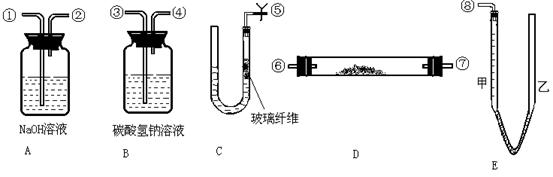
(1)图中装置的连接顺序是(填各接口的编号),其中连接胶管及夹持装置均省略:
______________________________________________。
(2)装置C中放入的反应物是________________和_____________。
(3)装置A的作用是_____________;装置B的作用是______________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意________和_______。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数。
c.读数时应上下移动乙管,使甲、乙两管液面相平。
d.读数时不一定使甲、乙两管液面相平。
查看习题详情和答案>>某课外活动小组模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。

图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0―50mL),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、大理石、水。试回答:
(1)图中装置的连接顺序是(填各接口的编号),其中连接胶管及夹持装置均省略):_______________________________________________。
(2)装置C中放入的反应物是________________和_____________。
(3)装置A的作用是_____________。装置B的作用是______________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意__________和_______(填写字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数。
c.读数时应上下移动乙管,使甲、乙两管液面相平。
d.读数时不一定使甲、乙两管液面相平。
查看习题详情和答案>>
(1)图中装置的连接顺序是(填各接口的编号),其中连接胶管及夹持装置均省略:
______________________________________________。
(2)装置C中放入的反应物是________________和_____________。
(3)装置A的作用是_____________;装置B的作用是______________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意________和_______。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数。
c.读数时应上下移动乙管,使甲、乙两管液面相平。
d.读数时不一定使甲、乙两管液面相平。
某学生课外活动小组模拟呼吸面具中的反应原理设计用图3-1所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
试回答:
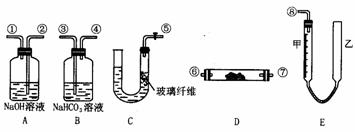
实验仪器
图3-1
(1)图中各装置接口连接顺序是______(填各接口的编号,其中连接胶管及夹持装置均省略)。
(2)装置C中放入的反应物是______和______。
(3)装置A的作用是______,装置B的作用是______。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中应注意______和______(填字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时立刻读数
c.读数时应上下移动乙管,使甲乙两管液面相平
d.读数时不一定使甲乙两管液面相平
查看习题详情和答案>>
某学生课外活动小组模拟呼吸面具中的反应原理设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装
入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。实验可供
选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。试回答:
(1)图中各装置接口连接顺序是______(填各接口的编号,其中连接胶管省略)。
(2)装置C中放入的反应物是______ 和______
(3)装置A的作用是______ ,装置B的作用是______
(4)装置组装完毕后应进行的操作是
(5)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后
甲管中液面的读数求其差值的过程中应注意___________(填字母编号)。
a.视线与凹液面最低处相平 b.待乙管中液面不再上升时立刻读数
c.读数时应上下移动乙管,使甲乙两管液面相平
查看习题详情和答案>>