摘要: 短周期元素X的氧化物.氢氧化物既能与强酸反应又能与强碱反应.其核外电子总数是内层电子总数的2倍,短周期元素Y的氢化物的浓的水溶液可与含Y的钾盐(KYO3)反应生成Y元素的单质.Y单质有毒.试根据以上信息完成下列问题: (1)写出X与Y形成的化合物的化学式 . (2)写出X的氧化物与Y的氢化物的水溶液反应的离子方程式 . (3)X的氧化物.氢氧化物所具备的特殊性质与另外一种与Y同周期的元素的氧化物.氢氧化物的性质相似.它们之所以相似.与它们在周期表中的相互位置有关.则下面说法合理的是 . A. 它们处于同一主族.故性质相似 B. 它们处于同一周期.并且相邻.故性质相似 C. 它们处于对角线的位置.故性质相似 D. 它们的最外层电子数都较少.故性质相似
网址:http://m.1010jiajiao.com/timu3_id_76535[举报]
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是
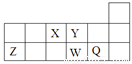
A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+)
B.元素W的最高价氧化物对应水化物的酸性比Q的强
C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
查看习题详情和答案>>
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是
| A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+) |
| B.元素W的最高价氧化物对应水化物的酸性比Q的强 |
| C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是
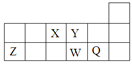

| A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+) |
| B.元素W的最高价氧化物对应水化物的酸性比Q的强 |
| C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
几种短周期元素的原子半径和主要化合价见下表:
元素代号 | X | Y | Z | L | M | Q |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
主要化合价 | +1 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
下列说法正确的是
A.在化学反应中,M原子既不容易失去电子,又不容易得到电子
B.等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多
C.Y与Q形成的化合物不可能跟氢氧化钠溶液反应
D.Z的氢化物的稳定性强于L的氢化物的稳定性
几种短周期元素的原子半径和主要化合价见下表:
元素代号 | X | Y | Z | L | M | Q |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
下列说法中,正确的是
A.在化学反应中,M原子既不容易失去电子,又不容易得到电子
B.等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多
C.Y与Q形成的化合物不可能跟氢氧化钠溶液反应
D.Z的氢化物的稳定性强于L的氢化物的稳定性