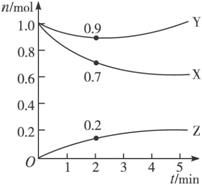
摘要:某温度时.在2 L容器中.X.Y.Z三种物质的物质的量随时间的变化曲线如图91所示.由图中数据分析.该反应的化学方程式为 ,反应从开始至2 min.Z的平均反应速率为 . 解析:在相同体积.相同时间内.反应速率之比等于物质的量变化之比. v∶Δn=∶∶=3∶1∶2,故该反应的化学计量数之比为3∶1∶2.且该反应为可逆反应. 答案:3X+Y2Z 0.05 mol·L-1·min-1
网址:http://m.1010jiajiao.com/timu3_id_76159[举报]
某温度时,在2 L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示。由图中数据分析:该反应的化学方程式为______。反应开始至2 min,用Z表示的平均反应速率为__________。

某温度时,在2 L 容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示。由图中数据分析:该反应的化学方程式为__________________________。反应开始至2 min,用Z表示的平均反应速率为______________。
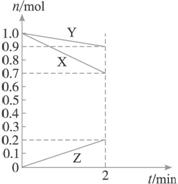
某温度时,在2 L 容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如下图所示。
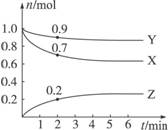
(1)由图中数据分析,该反应的化学方程式为________________________________________。
(2)反应开始至2 min,Z的平均反应速率为____________________。
(3)判断:第5分钟时,反应是否达到平衡?__________,第5分钟时,Z的生成速率比Z的消耗速率__________ (填“大”“小”或“相等”)。
查看习题详情和答案>>