网址:http://m.1010jiajiao.com/timu3_id_75521[举报]
在实验室中,下列除去杂质的方法不正确的是( )
A.溴苯中混有溴,加入碳酸钠溶液,振荡,然后分液
B.乙烷中混有乙烯,通入氢气,在一定条件下反应,使乙烯转化为乙烷
C.硝基苯中混有浓HNO3和浓H2SO4,将其倒入NaOH溶液中,静置,分液
D.乙烯中混有SO2和CO2,将其通入NaOH溶液中洗气
查看习题详情和答案>>
| A.溴苯中混有溴,加入碳酸钠溶液,振荡,然后分液 |
| B.乙烷中混有乙烯,通入氢气,在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓HNO3和浓H2SO4,将其倒入NaOH溶液中,静置,分液 |
| D.乙烯中混有SO2和CO2,将其通入NaOH溶液中洗气 |
在实验室中,下列除去杂质的方法不正确的是( )
| A.溴苯中混有溴,加入碳酸钠溶液,振荡,然后分液 |
| B.乙烷中混有乙烯,通入氢气,在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓HNO3和浓H2SO4,将其倒入NaOH溶液中,静置,分液 |
| D.乙烯中混有SO2和CO2,将其通入NaOH溶液中洗气 |
 Ⅰ.下列实验操作或对实验事实的描述不正确的是______ (填序号).
Ⅰ.下列实验操作或对实验事实的描述不正确的是______ (填序号).
①配制一定浓度的溶液时,俯视容量瓶的刻线,会使配制的浓度偏高
②向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
③仅用蒸馏水可鉴别出蔗糖、硫酸铜、碳酸钙三种粉末
④实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉
⑤测溶液大致的pH:用玻璃棒蘸取溶液滴在湿润的pH试纸上,与标准比色卡对照
Ⅱ.实验室有一份混有少量碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空[右图为Ba(OH)2和Ca(OH)2的溶解度曲线]:
(1)高温灼烧碳酸钡和碳酸钙的混合物,直至完全分解.所需仪器除三脚架、泥三角、酒精灯外,还需要的仪器有______、______、______;
(2)将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液.为减少Ba(OH)2的损失并除去不溶物得到Ba(OH)2固体,写出所进行的主要操作步骤的名称______、______、过滤;
(3)将(2)中得到的Ba(OH)2固体溶于水制成溶液再往其中滴入2滴酚酞,通入CO2,请简述Ba(OH)2恰好全部生成碳酸钡沉淀的判断方法______;
(4)滤出碳酸钡沉淀,经______后即得到纯净的碳酸钡.
查看习题详情和答案>>
(14分)FeSO4·7H2O广泛用于医药和工业领域,以下是FeSO4·7H2O的实验室制备流程图。根据题意完成下列填空:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_____,浸泡后,用____(填操作方法)分离并洗涤铁屑。
(2)操作a为_______________。
(3)最后得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;
②____________________。
(4) FeSO4·7H2O是某些补血剂的主要成分,实验室要测定某补血剂中铁元素的含量。
I.方案一:可用KMn04溶液进行氧化还原滴定。在配制100mL 1.00 × 10 - 2 mol·L-1的KMnO4溶液时,所用的仪器有天平、药匙、烧杯、玻璃棒,还有___________(填仪器名称)。在配制过程中,下列说法正确的是____________(填序号字母)。
A.KMnO4溶于水不放热,可以直接在容量瓶中溶解
B.容量瓶洗涤后不需干燥即可直接用于实验
C.定容后摇匀,凹液面低于刻度线,再加水至凹液面最低点与刻度线相平
D.如果定容时加水超过刻度线必须毓配制
II.方案二:将FeSO4·7H2O最终转化为Fe2O3,测定质量变化,操作流程如下:
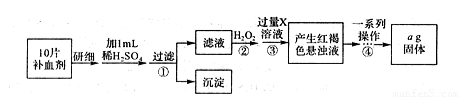
①步骤④中一系列操作依次是:过滤、洗涤、______、冷却、称量。
②假设实验过程中Fe无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示)。
③若步骤③加入X溶液的量不足,则最后测出每片补血剂含铁元素的质量将______(填“偏大,’.“偏小”或“不变”)。
查看习题详情和答案>>