摘要:9.下列说法中.正确的是( ) A.ΔH>0 kJ/mol表示放热反应.ΔH<0 kJ/mol表示吸热反应 B.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 C.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 D.热化学方程式中的化学计量数表示物质的量.所以可以是分数 解析:热化学方程式中的化学计量数表示物质的量.可以是整数.也可是以分数.ΔH>0表示吸热反应.ΔH<0表示放热反应.中和热和燃烧热的标准不同.中和热是稀溶液中酸和碱发生中和反应而生成1 mol H2O时的反应热,燃烧热是25 ℃.101 kPa时.1 mol纯物质完全燃烧生成稳定化合物时放出的热量. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_75491[举报]
化合物A经李比希法和质谱法得知其相对分子质量为136,分子式C8H8O2.A分子中只含有一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图.
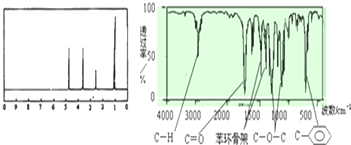
(1)A的分子中有 种不同化学环境的氢原子,关于A的下列说法中,正确的是
①A属于酯类化合物,在一定条件下能发生水解反应
②A不能和H2加成反应
③A不能和NaOH溶液发生反应
④符合题中A分子结构特征的有机物只有一种.
查看习题详情和答案>>

(1)A的分子中有
①A属于酯类化合物,在一定条件下能发生水解反应
②A不能和H2加成反应
③A不能和NaOH溶液发生反应
④符合题中A分子结构特征的有机物只有一种.
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
查看习题详情和答案>>
下列说法中,正确的是( )
A.强极性键形成的化合物不一定是强电解质
B.强电解质溶液的导电能力一定比弱电解质溶液强
C.NaCl溶液在电流的作用下电离成钠离子和氯离子
D.氯化钠晶体不导电是由于氯化钠晶体中不存在离子
查看习题详情和答案>> 3CO2+4H2O。下列说法中不正确的是
3CO2+4H2O。下列说法中不正确的是