摘要:11.已知反应:2SO2(g)+O2(g) 2SO3(g),ΔH<0.某温度下.将2 mol SO2和1 mol O2置于10 L密闭容器中.反应达平衡后.SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是 ( ) A.由图甲知.A点SO2的平衡浓度为0.4 mol·L-1 B.由图甲知.B点SO2.O2.SO3的平衡浓度之比为2?1?2 C.达平衡后.缩小容器容积.则反应速率变化图像可以用图乙表示 D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图.则T2>T1 答案:C
网址:http://m.1010jiajiao.com/timu3_id_75233[举报]
 已知反应:①2H2S+O2→2S+2H2O
已知反应:①2H2S+O2→2S+2H2O ②2H2S+SO2→3S+2H2O
③2H2S+3O2→2SO2+2H2O
将点燃的H2S气体的导管伸入盛有一定量O2的集气瓶内,上述3个反应发生的先后顺序是( )
查看习题详情和答案>>
哈三中某课外活动小组改进铜与浓硫酸反应的实验,制备并验证二氧化硫的性质,请回答下列问题:
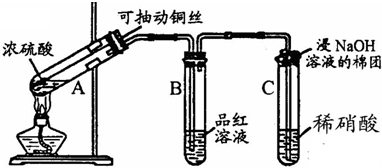
(1)铜丝在实验中的作用:
(2)实验过程中在装置C中会看到什么现象?
(3)已知反应:2SO2(g)+O2(g) 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
A.混合气体密度保持不变
B.c(SO2):c(O2):c(SO3)=2:1:2
C.容器内气体分子总数不随时间变化
D.相同时间内,消耗2n mol SO2的同时消耗n mol O2
(4)将0.23mol SO2和0.11mol O2放入容积为1L的密闭容器中,在一定温度下,经过2min反应达到平衡,得到0.12mol SO3.则用SO2浓度变化来表示反应速率为υ(SO2)=
若此时保持温度不变,同时通入0.12mol SO3和 0.15mol O2,则平衡
但若保持温度不变,只通入1.00mol O2,则重新达到平衡时,SO2的平衡浓度
查看习题详情和答案>>

(1)铜丝在实验中的作用:
控制反应的开始和停止
控制反应的开始和停止
.(2)实验过程中在装置C中会看到什么现象?
生成无色气体并变为红棕色
生成无色气体并变为红棕色
;请用化学方程式解释:SO2+HNO3=H2SO4+NO2NO+02=2NO2
SO2+HNO3=H2SO4+NO2NO+02=2NO2
.(3)已知反应:2SO2(g)+O2(g)
 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是C
C
.A.混合气体密度保持不变
B.c(SO2):c(O2):c(SO3)=2:1:2
C.容器内气体分子总数不随时间变化
D.相同时间内,消耗2n mol SO2的同时消耗n mol O2
(4)将0.23mol SO2和0.11mol O2放入容积为1L的密闭容器中,在一定温度下,经过2min反应达到平衡,得到0.12mol SO3.则用SO2浓度变化来表示反应速率为υ(SO2)=
0.06mol/L?min-1
0.06mol/L?min-1
.若此时保持温度不变,同时通入0.12mol SO3和 0.15mol O2,则平衡
不移动
不移动
(填“正向移动”、“逆向移动”、“不移动”、“无法确定”).但若保持温度不变,只通入1.00mol O2,则重新达到平衡时,SO2的平衡浓度
减小
减小
.(填“填大”、“不变”或“减小”),O2的转化率减小
减小
(填“升高”、“不变”或“降低”),SO2的体积分数减小
减小
(填“增大”、“不变”或“减小”).已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )

查看习题详情和答案>>
已知反应:2SO2(g)+O2(g) 2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

| A.由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |