摘要:20.A.B.C.D.E.F六种短周期主族元素.原子序数依次增大.其中B的单质在常温下为双原子分子.它与A的单质可形成分子X.X的水溶液呈碱性,D的简单阳离子与X具有相同电子数.且D是同周期中简单离子半径最小的元素,E元素的原子最外层比次外层少两个电子.C.F两种元素的原子最外层共有13个电子.则 (1)B的原子结构示意图 , (2)B.C.E分别与A形成的化合物中最稳定的是 , (3)C与D形成的化合物的化学式是 .它的性质决定了它在物质的分类中应属于 ,请写出该化合物的水化物的电离方程式 , (4)F的单质在反应中常作 剂.该单质的水溶液与E的低价氧化物反应的离子方程式为 . 解析:根据X的水溶液显碱性.得到B为N.A为H,D的简单阳离子为10e-结构.且在同周期简单离子中半径最小.推出D为Al元素,E 次外层电子数必须大于2.则E的核外电子排布为.E为S元素,F的原子序数比E大且为主族元素.F只能是Cl元素.即可推出C为O元素.其余可迎刃而解. 答案:(1) (2)H2O (3)Al2O3 两性氧化物 H2O+H++AlOAl(OH)3Al3++3OH- (4)氧化 SO2+Cl2+2H2O===4H++SO+2Cl-
网址:http://m.1010jiajiao.com/timu3_id_74780[举报]
A、B、C、D、E、F六种短周期元素,其原子序 数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素.又知六种元素所形成的常见单质在常 温常压下有三种是气体,三种是固体.
请回答下列问题:
(1)元素D在周期表中的位置 .
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有 .
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式: .
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式 .
查看习题详情和答案>>
请回答下列问题:
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式
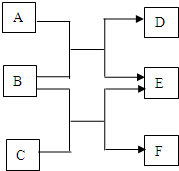 A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.
A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.(1)若A、C、E均为氧化物,且E为有毒气体,B、D、F均为非金属单质,且D为气体,则:
①F的晶体类型为
原子晶体
原子晶体
; 1molC中含有4
4
mol共价键;②B与C反应生成E和F的化学方程式为
2C+SiO2
Si+2CO
| ||
2C+SiO2
Si+2CO
| ||
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中A的相对分子质量最小;D、E、F皆为氧化物,且D、F皆为有毒气体.则:
①A、C、E三种氢化物沸点从高到低的顺序为
H2O>NH3>H2S
H2O>NH3>H2S
(填化学式);②A和F在水溶液中充入O2充分反应生成一种正盐,该反应的化学方程式为
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
(3)若B是由短周期元素组成的离子化合物,A、C为氧化物,E为气体单质,D、F是均有三种元素组成的离子化合物,它们的水溶液均呈碱性,相同浓度时D溶液的pH大于F.
①写出B的电子式


②B和C反应生成E和F的化学方程式
2Na2O2+2CO2=Na2CO3+O2
2Na2O2+2CO2=Na2CO3+O2
,列举该反应的一种用途呼吸面具和潜水艇中做为氧气的来源
呼吸面具和潜水艇中做为氧气的来源
.有A、B、C、D、E、F六瓶未知溶液.它们是MgSO4、BaCl2、(NH4)2CO3、AgNO3、HBr和NaOH.为了鉴别,各取少许溶液进行两两混和试验,结果如右表.表中“↓“表示有沉淀或生成微溶化合物,“↑“表示有气体生成,“-“表示观察不到明显的现象变化.由此可以判断:
A是 、B是 、C是 、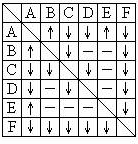
D是 、E是 、F是 .
查看习题详情和答案>>
A是

D是
A、B、C、D、E、F六种原子序数依次增大的短周期元素.A与其余五种元素既不同周期,也不同主族;B、C、D、E、F五种元素分别位于五个相邻的主族,原子序数之和为54;其中C、D原子的s能级和p能级电子总数均相等.
(1)D、E的第一电离能大小关系 (用元素符号表示)
(2)A、B形成的化合物液态时可发生微弱电离,电离产生的阴离子的电子式为 .
(3)某含F的盐矿石的组成可以看作其氧化物中有
的F被E替换,再由D平衡其电荷形成的.该矿石的化学式为 .(用氧化物形式表示)
(4)若将一充满m mL BC2和C2混合气体的大试管倒立于A2C中,充分反应后,在相同条件下测得试管中余下n mL气体,则原混合气体中BC2的体积为 mL:
查看习题详情和答案>>
(1)D、E的第一电离能大小关系
(2)A、B形成的化合物液态时可发生微弱电离,电离产生的阴离子的电子式为
(3)某含F的盐矿石的组成可以看作其氧化物中有
| 1 | 4 |
(4)若将一充满m mL BC2和C2混合气体的大试管倒立于A2C中,充分反应后,在相同条件下测得试管中余下n mL气体,则原混合气体中BC2的体积为
元素周期表、平衡移动原理是化学反应原理中的重要内容.请回答下列问题:现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)①A~F六种元素原子,原子半径最大的是
②A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为:
 .
.
③B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
④A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为:
(2)在一定温度下,向一个体积为1.0L的密闭容器中,通入3mol SO2 和2mol O2及固体催化剂,使之反应:2SO2(g)+O2(g) 2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.
2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.
①加入3mol SO2 和2mol O2 发生反应,达到平衡时放出的热量为
②该温度下反应的平衡常数是
查看习题详情和答案>>
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)①A~F六种元素原子,原子半径最大的是
D
D
(填序号).②A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为:


③B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
HClO和NH3(NH3?H2O)
HClO和NH3(NH3?H2O)
.④A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)在一定温度下,向一个体积为1.0L的密闭容器中,通入3mol SO2 和2mol O2及固体催化剂,使之反应:2SO2(g)+O2(g)
 2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.
2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.①加入3mol SO2 和2mol O2 发生反应,达到平衡时放出的热量为
98.3KJ
98.3KJ
②该温度下反应的平衡常数是
0.167
0.167
.