摘要:2.将镁片.铝片平行插入到一定浓度的NaOH溶液中.用导线连接成闭合回路.该装置在工作时.下列叙述正确的是 ( ) A.镁比铝活泼.镁失去电子被氧化成Mg2+ B.铝是电池的负极.开始工作时溶液中会立即有白色沉淀生成 C.该装置的内.外电路中.均是电子的定向移动形成电流 D.该装置开始工作时.铝片表面的氧化膜可不必处理 解析:对NaOH溶液而言Al比Mg活泼.故Al为负极.Mg为正极.负极电极反应式为:Al+4OH--3e-===AlO+2H2O.故A.B两项均不正确,内电路是阴.阳离子定向移动形成电流.故C项不正确,Al表面氧化膜不必另外处理.溶液中NaOH即可使其溶解.故D项正确. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_72704[举报]
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
| A.镁比铝活泼,镁失去电子被氧化成Mg2+ |
| B.该装置开始工作时,铝片表面的氧化膜可不必处理 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成 |
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是

A.镁比铝活泼,镁失去电子被氧化成Mg2+
B.该装置开始工作时,铝片表面的氧化膜可不必处理
C.该装置的内、外电路中,均是电子的定向移动形成电流
D.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成
查看习题详情和答案>>
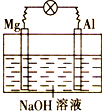 将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( ) A. 镁比铝活泼,镁失去电子被氧化成Mg2+
A. 镁比铝活泼,镁失去电子被氧化成Mg2+ 将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是