摘要:如图.利用一面墙.用80m长的篱笆围一个矩形场地. ⑴怎样围才能使矩形场地的面积为750m2? ⑵能否使所围矩形场地的面积为810m2.为什么?
网址:http://m.1010jiajiao.com/timu3_id_7205[举报]
32、某化学课外小组同学,用如图所示实验验证质量守恒定律.
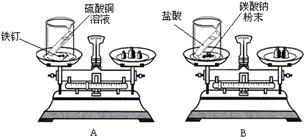
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上.
①发生反应的化学方程式为
②最后天平的指针(填序号)
(2)乙同学用B装置研究质量守恒定律,实验步骤如下: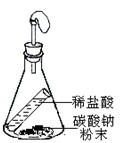
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上.发现天平的指针偏右.
①造成天平的指针向右偏转的原因是
②若将本实验中的烧杯替换成带有气球的锥形瓶,如图所示,其他操作不变,最后天平仍不平衡.可见,在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到
(3)在化学反应前后,一定不变的是(填序号)
①元素种类;②原子种类;③原子数目;④分子种类;⑤分子数目;⑥物质的总质量.
(4)应用质量守恒定律可以确定反应物或产物的化学式.在载人宇宙飞船中,一般都安装盛放过氧化钠(Na2O2)颗粒的装置,它的作用是再生氧气,供宇航员呼吸,反应的化学方程式为2 Na2O2+2CO2=2X+O2.则X的化学式为
(5)已知化学反应A+3B=2C+2D.在密闭容器中放入A、B、C、D,在一定条件下反应一段时间后,测得容器内各物质质量如表:
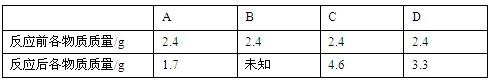
则B和C的相对分子质量之比为
查看习题详情和答案>>

(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上.
①发生反应的化学方程式为
Fe+CuSO4═FeSO4+Cu
.②最后天平的指针(填序号)
c
(a.偏左b.偏右c.不偏转d.无法预测).(2)乙同学用B装置研究质量守恒定律,实验步骤如下:

如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上.发现天平的指针偏右.
①造成天平的指针向右偏转的原因是
盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小
.②若将本实验中的烧杯替换成带有气球的锥形瓶,如图所示,其他操作不变,最后天平仍不平衡.可见,在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到
装置密闭,体积不变
.(3)在化学反应前后,一定不变的是(填序号)
①②③⑥
.①元素种类;②原子种类;③原子数目;④分子种类;⑤分子数目;⑥物质的总质量.
(4)应用质量守恒定律可以确定反应物或产物的化学式.在载人宇宙飞船中,一般都安装盛放过氧化钠(Na2O2)颗粒的装置,它的作用是再生氧气,供宇航员呼吸,反应的化学方程式为2 Na2O2+2CO2=2X+O2.则X的化学式为
Na2CO3
.(5)已知化学反应A+3B=2C+2D.在密闭容器中放入A、B、C、D,在一定条件下反应一段时间后,测得容器内各物质质量如表:

则B和C的相对分子质量之比为
8:11
. 24、化学与我们的生活是密切相关的,学好化学能提高我们的生活质量.结合化学知识回答下列问题:
24、化学与我们的生活是密切相关的,学好化学能提高我们的生活质量.结合化学知识回答下列问题:(1)小红妈为她买了一件漂亮的羊毛衫,标签内容如图所示:小红运用所学的化学知识,快速地确认了衣服的组成成分中确实含有羊毛,你认为小红采用的方法是
点燃后闻是否有烧焦羽毛味
.(2)中考复习期间,为让小明精力充沛,妈妈为他精心准备的午餐:米饭、煎蛋、清蒸鱼、红烧肉、豆腐汤.从“科学膳食”的角度分析,你认为这份午餐还需增加的食物有
新鲜水果、蔬菜
(填一种).(3)下表摘录的是矿泉水国家标准的部分内容:

从上表中可以看出:通过饮用矿泉水摄入的
硒
元素可以帮助人们增强防癌、抗癌的能力.(4)洗去餐具表面的油污,我们一般用洗涤剂,这是利用了
乳化
的原理.(2013?遵义)硫酸铜常用作农业杀虫剂,如图是利用含铁废铜料生产硫酸铜的工艺,回答下列问题.
(1)试剂X的化学式是
(2)途径II中,Cu+2H2SO4 (浓)
CuSO4+SO2↑+2H2O.从环保和经济的角度分析,利用途径
(填“Ⅰ”或“Ⅱ”)制取硫酸铜更合理;
(3)通常情况下不反应的两种物质,在改变温度和
A.小于6.4g B.等于6.4g C.大于6.4g.
查看习题详情和答案>>

(1)试剂X的化学式是
H2SO4
H2SO4
(2)途径II中,Cu+2H2SO4 (浓)
| ||
Ⅰ
Ⅰ
(填“Ⅰ”或“Ⅱ”)制取硫酸铜更合理;
(3)通常情况下不反应的两种物质,在改变温度和
反应物的浓度
反应物的浓度
后,也可能发生反应,如果用足量的铜与20.0溶质质量分数为98.0%的浓硫酸在加热条件下充分反应,实际生成二氧化硫的质量是A
A
(选填字母)A.小于6.4g B.等于6.4g C.大于6.4g.
某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究.(浓硫酸能干燥气体)
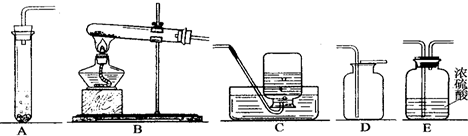
请你参与探究并回答下列问题.
(1)完成下表:
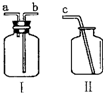 (2)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2).为了收集纯净的NO气体,利用如图所示仪器Ⅰ、Ⅱ,用胶管将
(2)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2).为了收集纯净的NO气体,利用如图所示仪器Ⅰ、Ⅱ,用胶管将
查看习题详情和答案>>

请你参与探究并回答下列问题.
(1)完成下表:
| 气 体 | 药 品 | 装置组合 | 化学方程式 | ||||||||
氧气(纯净) |
氯酸钾和二氧化锰 | B、C B、C |
2KClO3
2KClO3
| ||||||||
| 高锰酸钾 | B、C B、C |
2KMnO4
2KMnO4
| |||||||||
氧气(干燥) |
过氧化氢和二氧化锰 | A、E、D A、E、D |
2H2O2
2H2O2
|
 (2)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2).为了收集纯净的NO气体,利用如图所示仪器Ⅰ、Ⅱ,用胶管将
(2)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2).为了收集纯净的NO气体,利用如图所示仪器Ⅰ、Ⅱ,用胶管将b
b
(填导管口字母)与c相连组成收集装置.收集时,应先在Ⅰ中放水
水
(填物质名称).