摘要:7.已知X.Y.Z 3种主族元素在元素周期表中的相对位置如图所示.设X的原子序数为a.则下列说法中不正确的是 ( ) A.Y与Z的原子序数之和可能为2a B.Y的原子序数可能为a-19 C.Z的原子序数可能为a+33 D.X.Y.Z一定都是短周期元素 答案:D
网址:http://m.1010jiajiao.com/timu3_id_72019[举报]
已知X、Y、Z 3种主族元素在元素周期表中的相对位置如右图所示,设X的原子序数为a,则下列说法中不正确的是( )
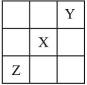
A.Y与Z的原子序数之和可能为2a B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31 D.X、Y、Z一定都是短周期元素
查看习题详情和答案>>已知X、Y、Z 3种主族元素在元素周期表中的相对位置如右图所示,设X的原子序数为a,则下列说法中不正确的是( )
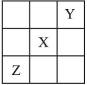

| A.Y与Z的原子序数之和可能为2a | B.Y的原子序数可能为a-17 |
| C.Z的原子序数可能为a+31 | D.X、Y、Z一定都是短周期元素 |
已知X、Y、Z 3种主族元素在元素周期表中的相对位置如右图所示,设X的原子序数为a,则下列说法中不正确的是
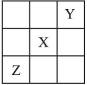
- A.Y与Z的原子序数之和可能为2a
- B.Y的原子序数可能为a-17
- C.Z的原子序数可能为a+31
- D.X、Y、Z一定都是短周期元素
已知X、Y、Z、W四种元素是元素周期表中连续三个短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的核外电子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z二种元素的元素符号:X
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为
 、
、
 、
、
 .
.
(3)由X、Y、Z所形成的常见离子化合物是
(4)在由X、Y、Z、W四种元素形成的常见化合物或单质中,不能形成的晶体类型是
查看习题详情和答案>>
(1)X、Z二种元素的元素符号:X
H
H
;ZO
O
.(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为






(3)由X、Y、Z所形成的常见离子化合物是
NH4NO3
NH4NO3
,它与W的最高价氧化物的水化物的浓溶液加热时反应的离子方程式NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(4)在由X、Y、Z、W四种元素形成的常见化合物或单质中,不能形成的晶体类型是
原子晶体
原子晶体
.已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.回答下列问题.
(1)X、Z二种元素的符号:X
(2)上述元素中形成的碱性氧化物的电子式为:
 ;
;
(3)由X、Y、Z所形成的常见离子化合物与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是:
(4)在由X、Y、Z、W四种元素形成的常见单质或化合物中,不能形成的晶体类型是
查看习题详情和答案>>
(1)X、Z二种元素的符号:X
H
H
、ZO
O
(2)上述元素中形成的碱性氧化物的电子式为:


(3)由X、Y、Z所形成的常见离子化合物与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是:
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(4)在由X、Y、Z、W四种元素形成的常见单质或化合物中,不能形成的晶体类型是
原子晶体
原子晶体
.