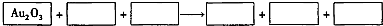摘要:5.某反应体系的物质有:NaOH.Au2O3.Na2S4O6.Na2S2O3.Au2O.H2O.下列选项正确的是( ). A.Na2S4O6.H2O.Na2S2O3.Au2O.NaOH B.Na2S2O3.NaOH.Na2S4O6.Au2O.H2O C.Na2S2O3.H2O.Na2S4O6.Au2O.NaOH D.当1mol Au2O3完全反应时.转移电子的物质的量为8mol [解析]选C.Au2O3是反应物.则Au2O一定是生成物.其中Au元素化合价由+3价变成+1价.化合价降低,.则必然有化合价升高的.即Na2S2O3是反应物.Na2S4O6是生成物.根据反应前后硫元素守恒则有:2Na2S2O3→Na2S4O6.根据钠元素守恒.则生成物这边缺少钠元素.所以NaOH是生成物.再根据氢元素守恒.则水是反应物.由关系式:Au2O3~Au2O~4e-.所以当1mol Au2O3完全反应时.转移电子的物质的量为4mol.
网址:http://m.1010jiajiao.com/timu3_id_71683[举报]
某反应体系的物质有:H2SO4、KMnO4、MnSO4、CO2、K2C2O4、K2SO4、H2O.(已知CO2为生成物)
(1)将上述物质填入以下空格内,组成一个配平的化学反应方程式,并标出电子转移数目.

(2)上述反应中,被氧化的元素是
(3)当有1mol的氧化剂参加反应时,转移的电子数是
查看习题详情和答案>>
(1)将上述物质填入以下空格内,组成一个配平的化学反应方程式,并标出电子转移数目.

(2)上述反应中,被氧化的元素是
碳
碳
,氧化产物是CO2
CO2
.(3)当有1mol的氧化剂参加反应时,转移的电子数是
5
5
mol.某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。

下列选项正确的是 ( )
A.框图中的物质分别为:Na2S4O6、H2O、Na2S2O3、Au2O、NaOH
B.框图中的物质分别为:Na2S2O3、NaOH、Na2S4O6、Au2O、H2O
C.框图中的物质分别为:Na2S2O3、H2O、Na2S4O6、Au2O、NaOH
D.当1 mol Au2O3完全反应时,转移电子的物质的量为6 mol
查看习题详情和答案>>