摘要:将足量的CO2慢慢通入一定体积某浓度的NaOH溶液中.溶液的pH随CO2体积的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化).则下列说法中不正确的是( ) A.NaOH溶液的物质的量浓度为0.1mol/L B.NaOH溶液的体积为2L C.M点粒子浓度的大小关系满足c(HCO3-)>c(CO32-) D.M.N点对应的纵坐标均大于7 [解析]选C.A项.NaOH溶液的pH为13.c(OH-)为0.1mol/L,B项.4.48L CO2物质的量为0.2mol.0.2mol CO2可与NaOH恰好完全反应生成NaHCO3 .所以NaOH溶液的体积为0.2mol÷ 0.1mol/L﹦2L.C项.M点对应 CO2物质的量为0.1mol.0.1 mol CO2可与NaOH恰好完全反应生成Na2CO3.溶液中粒子浓度的大小关系c(CO32-)>c(HCO3-),D项.M.N点对应的溶液中的溶质分别为 Na2CO3 .NaHCO3.两者水解都显碱性.pH大于7.
网址:http://m.1010jiajiao.com/timu3_id_71611[举报]
将足量的CO2慢慢通入一定体积的NaOH溶液中,溶液的pH随CO2的体积(已折算成标准状况)的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化),则下列说法正确的是

A.该NaOH溶液的体积为
B.该NaOH溶液的物质的量浓度为0.1 mol·L-1
C.M点时溶液中OH-的物质的量浓度为1×10-11 mol·L-1
D.N点溶液中的溶质为Na2CO3和NaHCO3,且二者物质的量之比为1∶2
查看习题详情和答案>>将足量的CO2慢慢通入一定体积的NaOH溶液中,溶液的pH随CO2的体积(已经折算成标准状况)的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化),则下列说法不正确的是
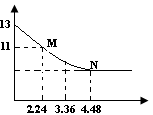
- A.NaOH溶液的物质的量浓度为0.1mol/L
- B.NaOH溶液的体积为2L
- C.M点离子浓度的大小关系满足c(HCO3-)>c(CO32-)
- D.M、N点对应的纵坐标均大于7
|
将足量的CO2慢慢通入一定体积的NaOH溶液中,溶液的pH随CO2的体积(已经折算成标准状况)的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化),则下列说法不正确的是
| |
| [ ] | |
A. |
NaOH溶液的物质的量浓度为0.1 mol/L |
B. |
NaOH溶液的体积为2 L |
C. |
M点粒子浓度的大小关系满足c(HCO3-)>c(CO32-) |
D. |
M、N点对应的纵坐标均大于7 |
将足量的CO2慢慢通入一定体积的NaOH溶液中,溶液的pH随CO2的体积(已经折算成标准状况)的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化),则下列说法不正确的是( )
| A.NaOH溶液的物质的量浓度为0.1mol/L |
| B.NaOH溶液的体积为2L |
| C.M点离子浓度的大小关系满足c(HCO3-)>c(CO32-) |
| D.M、N点对应的纵坐标均大于7 |

