摘要: 表示阿伏伽德罗常数.下列判断正确的是 ( ) A.在18中含有个氧原子 B.标准状况下.22.4L空气含有个单质分子 C.1 molCl2参加反应转移电子数一定为2 D.含个的溶解于1L水中.的物质的量浓度为1
网址:http://m.1010jiajiao.com/timu3_id_71400[举报]
由相同的两元素组成的四种粒子,1mol粒子内质子数分别是9NA、10NA、11NA、18NA(NA表示阿伏伽德罗常数),则这四种粒子的化学式分别是 、 、 、 (依上述顺序).
查看习题详情和答案>>
【化学--物质结构与性质】
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E的原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是 ,A、B、C、D的第一电离能由小到大的顺序为 ;
(2)B的氧化物的熔点远高于D的氧化物的熔点,理由是 ;
(3)A的最高价含氧酸根离子中,其中心原子是 杂化,D的低价氧化物分子的空间构型是 ;
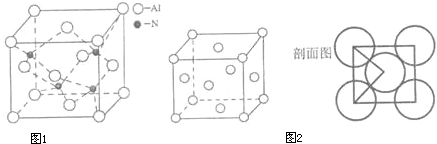
(4)A、C形成某种化合物的晶胞结构如图1所示,则其化学式为 ;(每个球均表示1个原子)
(5)铜晶体的晶胞结构如图2,若铜原子的半径是rcm,则铜的密度的计算式是 (用NA表示阿伏伽德罗常数).
查看习题详情和答案>>
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E的原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)

(1)E的核外电子排布式是
(2)B的氧化物的熔点远高于D的氧化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子是
(4)A、C形成某种化合物的晶胞结构如图1所示,则其化学式为
(5)铜晶体的晶胞结构如图2,若铜原子的半径是rcm,则铜的密度的计算式是