摘要:(09-10·福建福州八中高二下期中) .如图所示.甲.乙两池电极材料都是铁棒与碳棒.乙池中电子电子流动方向见图.回答下列问题: (1)若两池中均盛200mL饱和NaCl溶液和酚酞的混合液.反应开始后: ①甲池中 极.乙池中的 极附近溶液变红(填“正 或“负 或“阴 或“阳 ). ②甲池碳极上电极反应式是 乙池中Fe电极上反应式为 . ③若乙池中收集到1.12L有色气体时.停止实验.忽略池中溶液体积的变化.则池中溶液的c(OH-)约为 .要使溶液恢复到电解前的相同的状况.应向溶液中补充一定量的 A.盐酸 B. NaCl固体 C. NaCl溶液 D. HCl气体 (2)若两池中均盛有200mL 2mol•L-1CuSO4溶液: ①反应一段时间后.有红色物质析出的是甲池中的 棒.乙池中的 棒. ②写出乙池通电时总反应的离子方程式: . ③若乙池中通过1.2mol 电子后停止实验.则乙池中共可收集到气 体的体积为 . 答案: ③0.5mol•L-1.D ②2Cu2+ + 2H2OO2↑+ Cu2++ 4H+. ③6.72L
网址:http://m.1010jiajiao.com/timu3_id_71024[举报]
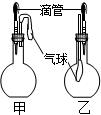 (2009?黄浦区二模)如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂可能是( ) (2009?黄浦区二模)如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂可能是( )
|
查看习题详情和答案>>
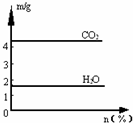 将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( ) 将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
|
查看习题详情和答案>>
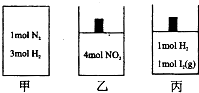 如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:
如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:甲:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol
乙:2NO2(g)?N2O4
丙:H2(g)+I2(g)?2HI(g)
则下列有关说法不正确的是( )
| A、若甲的体积为2L,经过10秒后反应达到平衡状态,放出热量为55.44U,则H2的反应速率是0.09mol/(L?s) | B、若甲、乙中反应达到平衡时的体积相同,则两容器中所含物质的量可能相同 | C、若乙、丙中反应达到平衡时的体积、压强均相同,则乙中NO2的转化率为50% | D、若甲、乙、丙中反应均达到平衡状态时,则甲中物质的平均相对分子质量不变,乙中物质的颜色不变,丙中的温度不变 |
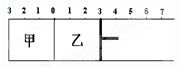 如图所示,甲容器容积固定不变,乙容器有可移动的活塞.甲中充入2mol SO2和1mol O2,乙中充入4mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)?2SO2(g)+O2 (g)下列有关说法正确的是( )
如图所示,甲容器容积固定不变,乙容器有可移动的活塞.甲中充入2mol SO2和1mol O2,乙中充入4mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)?2SO2(g)+O2 (g)下列有关说法正确的是( )