摘要:12.把含硫酸铵和硝酸铵的混合液a L分成两等份.一份加入bmol NaOH并加热.恰好把NH3全部赶出,另一份需消耗cmol BaCl2沉淀反应恰好完全.则原溶液中NO3- 的浓度为 ( ) A B C D 第II卷
网址:http://m.1010jiajiao.com/timu3_id_69721[举报]
把含硫酸铵和硝酸铵的混合液a L分成两等份.一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42-完全沉淀,则原溶液中NO3-的物质的量浓度为( )
把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42-完全沉淀,则原溶液中NO3-的物质的量浓度为
A. | B. | C.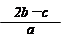 | D. |
把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42-完全沉淀,则原溶液中NO3-的物质的量浓度为
A. B.
B. C.
C.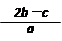 D.
D.
查看习题详情和答案>>
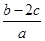 B、
B、 C、
C、 D、
D、
 B
B  C
C
 D
D
