摘要:14.某学习小组用如图所示装置测定加NaOH溶液镁合金中加NaOH溶液的质量分数和加NaOH溶液的相对原子质量. (1)A中试剂为 . (2)实验前.先将加NaOH溶液镁合金在稀酸中浸泡片刻.其目的是 . (3)检查气密性.将药品和水装入各仪器中.连接好装置后.需进行的操作还有:①记录C的液面位置,②将B中剩余固体过滤.洗涤.干燥.称重,③待B中不再有气体产生并恢复至室温后.记录C的液面位置,④由A向B滴加足量试剂,⑤检查气密性.上述操作的顺序是 ,记录C的液面位置时.除视线平视外.还应 . (4)B中发生反应的化学方程式为 . (5)若实验用加NaOH溶液镁合金的质量为a g.测得氢气体积为b mL.B中剩余固体的质量为c g.则加NaOH溶液的相对原子质量为 . (6)实验过程中.若未洗涤过滤所得的不溶物.则测得加NaOH溶液的质量分数将 (填“偏大 .“偏小 或“不受影响 ). 解析 (1)观察实验装置图可知是用量气法完成实验目的.故A中应盛NaOH溶液.在B中发生2Al+2NaOH+2H2O===2NaAlO2+3H2↑的反应. (2)目的是除去加NaOH溶液镁合金表面的氧化膜. (3)正确顺序应为⑤①④③②,为使C中气体的压强与外界大气压相等.还应使D与C的液面相平. (5)据2Al - 3H2 2 3 得M(Al)= (6)据w(Al)=×100%的计算公式可知未洗涤不溶物会造成加NaOH溶液的质量分数偏小. 答案 除去加NaOH溶液镁合金表面的氧化膜 (3)⑤①④③② 使D和C的液面相平 (4)2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 偏小
网址:http://m.1010jiajiao.com/timu3_id_69583[举报]
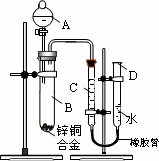
某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量.

(1)A中试剂为____________________.
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________.
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;
③待B中不 再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂;
上述操作的顺序是_________(填序号);记录C的液面位置时,除视线平视外,还应______________________
(4)B中发生反应的化学反应方程式__________________
(5)若实验 用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B 中剩余固体的质量为c g,则铝的相对原子质量为____________.
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________.(填“偏大”、“偏小”或“不受影响”)
查看习题详情和答案>>
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________.
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;
③待B中不 再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂;
上述操作的顺序是_________(填序号);记录C的液面位置时,除视线平视外,还应______________________
(4)B中发生反应的化学反应方程式__________________
(5)若实验 用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B 中剩余固体的质量为c g,则铝的相对原子质量为____________.
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________.(填“偏大”、“偏小”或“不受影响”)
| |||||||||||||||||||||||||||||||||||||
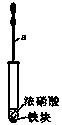 某化学学习小组用如图所示装置研究不同条件下铁与硝酸反应的情况.其实验步骤如下:
某化学学习小组用如图所示装置研究不同条件下铁与硝酸反应的情况.其实验步骤如下:①在大试管中先加入一小块铁(过量),再加入一定量的浓硝酸;
②用仪器a再加入适量的水;
③反应结束后取少量上层溶液于另一试管中,滴加几滴KSCN溶液;
④再用仪器a向③的试管中滴加适量的稀盐酸.
请回答下列问题:
(1)仪器a的名称是
(2)步骤①无明显现象,原因是
(3)步骤④的主要现象是
(4)学习小组在进行实验后发现该实验装置存在着一种明显的缺陷,请给出一种简单的消除此缺陷的措施:
 化学是一门以实验为基础的自然科学.
化学是一门以实验为基础的自然科学.(1)下列说法中,符合实验安全规范要求的是
①②
①②
(填序号字母).①闻气体的气味时,应用手在瓶口轻轻煽动,使少量的气体飘进鼻孔
②在实验室做铜和浓硝酸反应制备二氧化氮的实验时,应该在通风橱中进行
③做H2还原CuO实验时,先加热CuO至高温,然后立即通入H2使反应发生
④实验中当有少量的过氧化钠剩余时,用纸包裹好后将其放入垃圾桶中
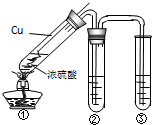
(2)某学习小组用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应及部分产物的性质(装置中的铜丝可适当上下抽动).
①当反应进行一段时间后,欲使反应迅速停止,可采取的措施为
向上(向外)抽动铜丝,使铜丝脱离浓硫酸
向上(向外)抽动铜丝,使铜丝脱离浓硫酸
.②若装置②用来检验生成的气体产物的性质,在装置②的试管中加入的试剂为品红试液,通入气体后,现象为
品红试液退色
品红试液退色
,此现象证明该气体产物具有漂白
漂白
性.③装置③中盛有某单质的水溶液,用来检验气体产物的还原性,则该单质的水溶液为
氯水
氯水
,反应的化学方程式为Cl2+SO2+2H2O=2HCl+H2SO4
Cl2+SO2+2H2O=2HCl+H2SO4
.④实验最后,要将图①大试管中的液体与水混合,以观察颜色检验存在的离子,从安全角度考虑,混合的方法应该是
将①中大试管中冷却后的部分液体沿烧杯内壁缓慢注入盛有适量水的烧杯中,并不断搅拌
将①中大试管中冷却后的部分液体沿烧杯内壁缓慢注入盛有适量水的烧杯中,并不断搅拌
.⑤实验中,在所用仪器及仪器间连接都完好的情况下,同学们仍闻到了较强的刺激性气味,说明此实验的整套装置设计有缺陷,会造成空气污染.改进此实验装置的方法是
在装置③处连一个装有NaOH溶液的洗气瓶,以吸收有毒尾气
在装置③处连一个装有NaOH溶液的洗气瓶,以吸收有毒尾气
.某课外研究性学习小组用如图所示装置制备少量溴苯并验证溴与苯的反应是取代反应.

实验时,关闭F火塞,打开C火塞,在装有少量苯的三口烧瓶中由A口加入少量溴,再加入铁屑,塞住A口.
回答下列问题:
(1)D试管中装的是什么
(2)E试管内装的是
(3)除去溴苯中混有的Br2杂质的试剂是
(4)三口烧瓶中发生反应的化学方程式为
(5)根据什么现象可证明验证溴与苯的反应是取代反应?
查看习题详情和答案>>

实验时,关闭F火塞,打开C火塞,在装有少量苯的三口烧瓶中由A口加入少量溴,再加入铁屑,塞住A口.
回答下列问题:
(1)D试管中装的是什么
CCl4
CCl4
,其作用是除去挥发出来的溴
除去挥发出来的溴
.(2)E试管内装的是
硝酸银溶液
硝酸银溶液
(3)除去溴苯中混有的Br2杂质的试剂是
氢氧化钠溶液
氢氧化钠溶液
,操作方法为向三口烧瓶中加入少量氢氧化钠溶液,振荡,转入分液漏斗,分液
向三口烧瓶中加入少量氢氧化钠溶液,振荡,转入分液漏斗,分液
.(4)三口烧瓶中发生反应的化学方程式为
2Fe+3Br2=2FeBr3
2Fe+3Br2=2FeBr3
,C6H6+Br2
C6H5Br+HBr
| FeBr3 |
C6H6+Br2
C6H5Br+HBr
.| FeBr3 |
(5)根据什么现象可证明验证溴与苯的反应是取代反应?
E中产生淡黄色沉淀
E中产生淡黄色沉淀
.