网址:http://m.1010jiajiao.com/timu3_id_68356[举报]
下面的排序不正确的是
A.晶体熔点由低到高:CF4< CCl4< CBr4< CI4
B.硬度由大到小:金刚石 > 碳化硅 > 晶体硅
C.熔点由高到低:Na > Mg > Al
D.晶体的熔点高低规律一般有:原子晶体 > 离子晶体 > 分子晶体
查看习题详情和答案>>
下面的排序不正确的是
- A.晶体熔点由低到高:CF4< CCl4< CBr4< Cl4
- B.硬度由大到小:金刚石 > 碳化硅 > 晶体硅
- C.熔点由高到低:Na > Mg > Al
- D.晶体的熔点高低规律一般有:原子晶体 > 离子晶体 > 分子晶体
下面的排序不正确的是
| A.晶体熔点由低到高:CF4< CCl4< CBr4< CI4 |
| B.硬度由大到小:金刚石 > 碳化硅 > 晶体硅 |
| C.熔点由高到低:Na > Mg > Al |
| D.晶体的熔点高低规律一般有:原子晶体 > 离子晶体 > 分子晶体 |
下列结论和解释均正确的是
| 选项 | 结 论 | 解释 |
| A | 稳定性:H2O>H2S | 因为水中有氢键 |
| B | 酸性:盐酸 > 氢硫酸 | 因为Cl的非金属性比S强 |
| C | 原子半径:B>Be | 因为B的核电荷数比Be大 |
| D | 熔沸点:原子晶体>分子晶体 | 因为共价键比分子间作用力强得多 |
[化学—物质结构与性质]
(1)依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。

(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 NF3+3NH4F
NF3+3NH4F
①上述化学方程式中的5种物质所属的晶体类型有_________(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
②基态铜原子的核外电子排布式为________。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

①晶体Q中各种微粒间的作用力不涉及___________(填序号)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
②R中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。
(4)已知苯酚( )具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子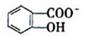 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
查看习题详情和答案>>