摘要:5.某温度下. 的平衡常数.该温度下在甲.乙.丙三个恒容密闭容器中.投入H2(g)和CO2(g).其起始浓度如右表所示.下列判断不正确的是w w w. k#s5 A.平衡时.乙中CO2的转化率大于60% B.平衡时.甲中和丙中H2的转化率均是60% C.平衡时.丙中c(CO2)是甲中的2倍.是0.012mol/L D.反应开始时.丙中的反应速率最快.甲中的反应速率最慢 解析:甲中设平衡时生成物的物质的量浓度为x.则有:.解得x=0.006.所以H2.CO2的转化率均为60%.此时CO2的浓度是0.004.反应前后体积不变.因此甲和丙中的平衡等效.B正确,由于容器的容积相同.所以平衡时.丙中c(CO2)是甲中的2倍.是0.008mol/L.C错,乙可以看作是在甲的基础上增大氢气的物质的量浓度.所以可以提高CO2的转化率.A正确,浓度越高.压强越大.反应越快.D正确, 答案:C
网址:http://m.1010jiajiao.com/timu3_id_67567[举报]
 12某温度下,
12某温度下, ![]() 的平衡常数
的平衡常数![]() .该温度下在甲、乙、丙三个恒容密闭容器中,
.该温度下在甲、乙、丙三个恒容密闭容器中,
投入H2(g)和CO2(g),其起始浓度如右表所示。下列判断不正确的是
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
查看习题详情和答案>>某温度下, 的平衡常数
的平衡常数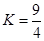 .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
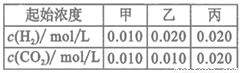
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看习题详情和答案>>
某温度下, ![]() 的平衡常数
的平衡常数![]() .该温度下在甲、乙、丙三个恒容密闭容器中,
.该温度下在甲、乙、丙三个恒容密闭容器中,
投入H2(g)和CO2(g),其起始浓度如右表所示。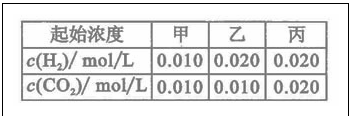 下列判断不正确的是
下列判断不正确的是
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看习题详情和答案>>某温度下,![]() 的平衡常数
的平衡常数![]() .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
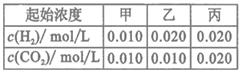
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看习题详情和答案>>某温度下,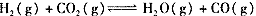 的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表 所示。 的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表 所示。 |
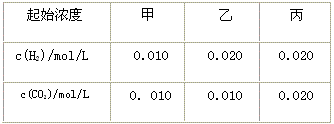 |
| 下列判断不正确的是 |
|
[ ] |
| A.平衡时,乙中CO2的转化率大于60% B.平衡时,甲中和丙中H2的转化率均是60% C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |