摘要:9. (1)第二周期VIA族,O N Na 催化剂 .NH+4+H2ONH3·H2O+H+ △ (3)4NH3+5O2====== 4NO+6H2O (4)1:1010(或10-10.10-10:1)
网址:http://m.1010jiajiao.com/timu3_id_66143[举报]
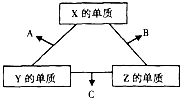 X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:(1)X元素在周期表中的位置是
第二周期VIA族
第二周期VIA族
.Y的原子序数为7
7
.(2)X的单质与Z的单质可制成新型的化学电源,该电源被称为
氢氧燃料电池
氢氧燃料电池
.(3)A的化学式为
NO
NO
.(4)已知Y的单质与Z的单质在适当催化剂和高温、高压条件下,生成C的反应是可逆反应,写出该反应的化学方程式
N2+3H2
2NH3
| 高温、高压 |
| 催化剂 |
N2+3H2
2NH3
.| 高温、高压 |
| 催化剂 |
有W、X、Y、Z四种短周期元素,它们的核电荷数依次增大; W元素原子是所有原子中半径最小的; X元素原子L层电子数是K层电子数的3倍,Y元素原子的最外层电子数与电子层数相同;Z元素原子的最外层电子数比次外层少1.由此可知:
(1)写出它们的元素符号W
(2)X在元素周期表中的位置是
查看习题详情和答案>>
(1)写出它们的元素符号W
H
H
XO
O
YAI
AI
ZCl
Cl
.(2)X在元素周期表中的位置是
第二周期 VIA族
第二周期 VIA族
.A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大.A、D同主族;B、D、E三种元素原子的最外层电子数之和为9.又知B、D、E分别与A、C两元素共同组成的三种化合物X、Y、Z之间能相互发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M,1molM中含有42mol电子.回答下列问题:
(1)元素C在周期表中的位置是
(2)化合物M中含有的化学键类型有
(3)写出化合物Y与Z之间反应的离子方程式
(4)以铂作电极,以Y溶液作为电解质溶液,A、C元素的单质分别在两电极上发生原电池反应,则正极上的电极反应式为
查看习题详情和答案>>
(1)元素C在周期表中的位置是
第二周期 VIA族
第二周期 VIA族
;(2)化合物M中含有的化学键类型有
离子键、共价键
离子键、共价键
;(3)写出化合物Y与Z之间反应的离子方程式
A1(OH)3+OH-=A1O2-+2H2O
A1(OH)3+OH-=A1O2-+2H2O
;(4)以铂作电极,以Y溶液作为电解质溶液,A、C元素的单质分别在两电极上发生原电池反应,则正极上的电极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
现有八种短周期元素a—h的有关性质的数据如下:
元素编号 | a | b | c | d | e | f | g | h |
原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
根据元素周期律,判断下列推断不正确的是( )
A.元素a与元素c形成的化合物分子中的化学键是极性键
B.b元素形成的氢化物分子间存在氢键
C.e元素位于元素周期表中的第二周期VIA族
D.元素f的最高价氧化物的水化物能溶于元素h的最高价氧化物的水化物的水溶液中