摘要: .铝热反应.焊接铁轨.冶炼金属, 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O (2)6H2O +6e - =3H2↑+6OH - ②:2SO2+O22SO3 ③:2Fe+6H2SO4(浓) Fe2(SO4)3+3SO2↑+6H2O
网址:http://m.1010jiajiao.com/timu3_id_66138[举报]
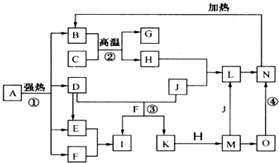 仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:
仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:(1)反应①既是分解反应,又是氧化还原反应,产物B、D、E、F的物质的量之比1:1:1:14.A强热分解的化学反应方程式为
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
| ||
. |
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
.
| ||
. |
(2)写出反应②在工业生产上的一种用途:
焊接钢轨
焊接钢轨
.(3)反应③的离子方程式为
Cl2+SO2+2H2O═4H++SO42-+2Cl-
Cl2+SO2+2H2O═4H++SO42-+2Cl-
;反应④的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
.(4)常以C或H制成容器盛装和运输I的浓溶液,其原理是
冷的浓硫酸与铁或铝制容器接触时,在表面生成一层致密的氧化膜,阻止金属继续与酸反应而使金属“钝化”,所以可用铁或铝制容器储运浓硫酸
冷的浓硫酸与铁或铝制容器接触时,在表面生成一层致密的氧化膜,阻止金属继续与酸反应而使金属“钝化”,所以可用铁或铝制容器储运浓硫酸
.