网址:http://m.1010jiajiao.com/timu3_id_66125[举报]
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下: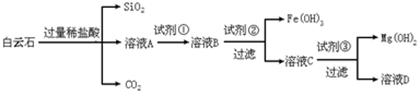
实验过程中需要的数据见下表:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
| A.KMnO4 | B.Cl2 | C.MgO | D.CaO |
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:
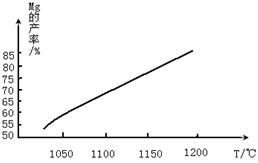
煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。 查看习题详情和答案>>
白云石的主要成分为CaCO3?MgCO3,还含有少量Fe、Si的化合物.实验室以白云石为原料制备Mg(OH)2及CaCO3.步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
(1)过滤中所需的玻璃仪器是______,溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择______(填字母,下同).
A.KMnO4 B.Cl2 C.H2O2
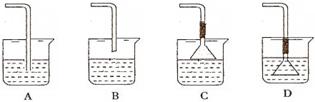
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是______,然后通入CO2.通入CO2气体时请把装置图补充完整______(不允许更换溶液,导气管以下连接的仪器自选)

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为______.
(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是______. 查看习题详情和答案>>
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:

煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看习题详情和答案>>白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:
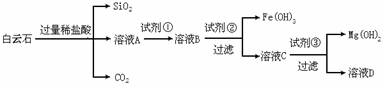
实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。
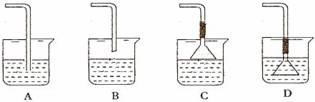
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:
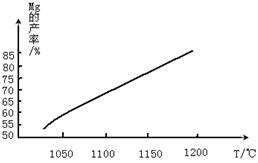
煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看习题详情和答案>>白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:

煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看习题详情和答案>>