网址:http://m.1010jiajiao.com/timu3_id_65885[举报]
A.有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z.E、Q、T三种元素的基态原子具有相同的能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT+2与ET2互为等电子体.X为周期表前四周期中电负性最小的元素,Z的原子序数为28.
请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT+2的电子式


(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有
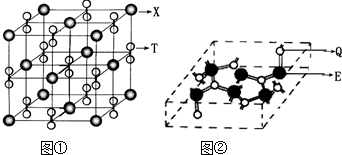
(3)化合物甲由T、X两种元素组成,其晶胞如图①,甲的化学式为
(4)化合物乙的晶胞如图②,乙由E、Q两种元素组成,硬度超过金刚石.
①乙的晶体类型为
②乙的晶体中E、Q两种元素原子的杂化方式均为
B.现有氧化铜和碳粉组成的混合物,为通过实验确定氧化铜的质量分数,某同学设计的实验方案中装置如下:
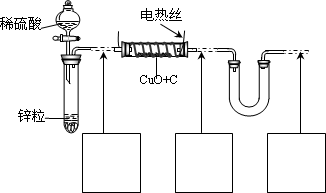
分析上述装置,回答下列问题:
(1)本实验中,酒精灯加热也可达到反应所需的温度,改用电热丝加热的优点是有利于
a.加快反应速率b.氢气流动
c.加热温度更高d.精确测定数据
(2)为确保能准确测定到必要的数据,下列步骤按实验操作顺序排列应为:
a.停止通氢气;b.电热丝通电;c.通入氢气;d.装置气密性检查;e.电热丝停止通电.
(3)为准确测定数据,你认为本装置是否完整?若需要改进,请在虚线下面的方框内画出所需添加的装置示意图并注明必要的物质名称.若无需改进,则将装置图中虚线部分改为实线.
(4)实验结束后,该同学交给老师的实验报告主要栏目如图

(具体内容已略).请你根据实验报告的撰写要求,对此份报告作出评价,若有不完整,请在下面的空格中写出,若已完整,则无需填写.
(5)老师看完实验报告后指出,改变实验原理可以设计出更加简便的实验方案.请你用化学方程式来表示新方案的反应原理,并指出需要测定的数据:
化学方程式
| 高温 |
| 高温 |
需要测定的数据
(12分)X、Y、Z、L、M五种短周期元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,其中X是原子半径最小的元素,L是地壳中含量最高的元素 。M是地壳中含量最高的金属元素。回答下列问题:⑴Z的单质一个分子中含有____个π键 ; M的原子结构示意图为_______________
(2)五种元素原子半径从大到小的顺序是________________________(用元素符号表示)
(3) Y、Z、L三种元素第一电离能由大到小的顺序是______________(用元素符号表示)
(4) Z、X两元素按原子数目比l∶3和2∶4分别构成分子A和B,A分子空间构型为___________,A分子中Z原子的轨道杂化方式为_______,B的结构式为______________。
(5) 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为_____________。
该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
查看习题详情和答案>>
(12分)X、Y、Z、L、M五种短周期元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,其中X是原子半径最小的元素,L是地壳中含量最高的元素 。M是地壳中含量最高的金属元素。回答下列问题:⑴Z的单质一个分子中含有____个π键; M的原子结构示意图为_______________
(2)五种元素原子半径从大到小的顺序是________________________(用元素符号表示)
(3) Y、Z、L三种元素第一电离能由大到小的顺序是______________(用元素符号表示)
(4) Z、X两元素按原子数目比l∶3和2∶4分别构成分子A和B,A分子空间构型为___________,A分子中Z原子的轨道杂化方式为_______,B的结构式为______________。
(5) 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为_____________。
该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
查看习题详情和答案>>
(12分)X、Y、Z、L、M五种短周期元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,其中X是原子半径最小的元素,L是地壳中含量最高的元素。M是地壳中含量最高的金属元素。回答下列问题:⑴Z的单质一个分子中含有____个π键; M的原子结构示意图为_______________
(2)五种元素原子半径从大到小的顺序是________________________(用元素符号表示)
(3) Y、Z、L三种元素第一电离能由大到小的顺序是______________(用元素符号表示)
(4) Z、X两元素按原子数目比l∶3和2∶4分别构成分子A和B,A分子空间构型为___________,A分子 中Z原子的轨道杂化方式为_______,B的结构式为______________。
中Z原子的轨道杂化方式为_______,B的结构式为______________。
(5) 硒(se)是人体必需的微量元素 ,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为_____________。
,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为_____________。
该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1 b.+29.7  mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
X、Y、Z、L、M五种短周期元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,其中X是原子半径最小的元素,L是地壳中含量最高的元素.M是地壳中含量最高的金属元素.回答下列问题:
(1)Z的单质一个分子中含有________个π键;M的原子结构示意图为________
(2)五种元素原子半径从大到小的顺序是________(用元素符号表示)
(3)Y、Z、L三种元素第一电离能由大到小的顺序是________(用元素符号表示)
(4)Z、X两元素按原子数目比l∶3和2∶4分别构成分子A和B,A分子空间构型为________,A分子中Z原子的轨道杂化方式为________,B的结构式为________.
(5)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为________.
该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是________(填字母代号).
a.+99.7 mol·L-1
b.+29.7 mol·L-1
c.-20.6 mol·L-1
d.-241.8 kJ·mol-1