摘要:可能改变的是:①分子的数目②元素的化合价.
网址:http://m.1010jiajiao.com/timu3_id_6468[举报]
(1)质量守恒定律是我们化学学习中一个非常重要的工具,质量守恒定律的本质是化学反应前后
①物质种类 ②元素种类和质量 ③原子的数目 ④原子的种类 ⑤原子的质量 ⑥分子种类 ⑦分子的数目
(2)已知铜绿的化学式为Cu2(OH)2CO3,将铜绿加强热后完全分解,发生反应可表示为:Cu2(OH)2CO3
CO2+H2O+X
已知X为黑色的粉末,且为纯净物.因此甲乙丙三位同学分别作出了猜想:
甲同学认为X是碳粉.
乙同学认为X是氧化铜.
丙同学认为X是二氧化锰.
你认为
(3)如图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验.请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为ag、混合后质量均为bg):
①甲组药品混合前、后质量关系为:ag
②乙组药品混合前、后质量关系为:ag
③丙组同学认为乙组同学实验成功,能用于验证质量守恒定律.
你认为丙组同学对吗?为什么?

查看习题详情和答案>>
②③④⑤
②③④⑤
没有改变(请选择以下合适的序号填空)①物质种类 ②元素种类和质量 ③原子的数目 ④原子的种类 ⑤原子的质量 ⑥分子种类 ⑦分子的数目
(2)已知铜绿的化学式为Cu2(OH)2CO3,将铜绿加强热后完全分解,发生反应可表示为:Cu2(OH)2CO3
| 加热 |
已知X为黑色的粉末,且为纯净物.因此甲乙丙三位同学分别作出了猜想:
甲同学认为X是碳粉.
乙同学认为X是氧化铜.
丙同学认为X是二氧化锰.
你认为
乙
乙
同学猜想正确.(3)如图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验.请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为ag、混合后质量均为bg):
①甲组药品混合前、后质量关系为:ag
大于
大于
bg,(选择大于或小于或等于填空)②乙组药品混合前、后质量关系为:ag
等于
等于
bg,(选择大于或小于或等于填空)③丙组同学认为乙组同学实验成功,能用于验证质量守恒定律.
你认为丙组同学对吗?为什么?
不对,因为乙组的两种药品未参加化学反应,所以不能验证质量守恒定律
不对,因为乙组的两种药品未参加化学反应,所以不能验证质量守恒定律

(1)质量守恒定律是我们化学学习中一个非常重要的工具,质量守恒定律的本质是化学反应前后 没有改变(请选择以下合适的序号填空)
①物质种类 ②元素种类和质量 ③原子的数目 ④原子的种类 ⑤原子的质量 ⑥分子种类 ⑦分子的数目
(2)已知铜绿的化学式为Cu2(OH)2CO3,将铜绿加强热后完全分解,发生反应可表示为:Cu2(OH)2CO3 CO2+H2O+X
CO2+H2O+X
已知X为黑色的粉末,且为纯净物.因此甲乙丙三位同学分别作出了猜想:
甲同学认为X是碳粉.
乙同学认为X是氧化铜.
丙同学认为X是二氧化锰.
你认为 同学猜想正确.
(3)如图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验.请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为ag、混合后质量均为bg):
①甲组药品混合前、后质量关系为:ag bg,(选择大于或小于或等于填空)
②乙组药品混合前、后质量关系为:ag bg,(选择大于或小于或等于填空)
③丙组同学认为乙组同学实验成功,能用于验证质量守恒定律.
你认为丙组同学对吗?为什么?
 查看习题详情和答案>>
查看习题详情和答案>>
①物质种类 ②元素种类和质量 ③原子的数目 ④原子的种类 ⑤原子的质量 ⑥分子种类 ⑦分子的数目
(2)已知铜绿的化学式为Cu2(OH)2CO3,将铜绿加强热后完全分解,发生反应可表示为:Cu2(OH)2CO3
 CO2+H2O+X
CO2+H2O+X已知X为黑色的粉末,且为纯净物.因此甲乙丙三位同学分别作出了猜想:
甲同学认为X是碳粉.
乙同学认为X是氧化铜.
丙同学认为X是二氧化锰.
你认为 同学猜想正确.
(3)如图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验.请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为ag、混合后质量均为bg):
①甲组药品混合前、后质量关系为:ag bg,(选择大于或小于或等于填空)
②乙组药品混合前、后质量关系为:ag bg,(选择大于或小于或等于填空)
③丙组同学认为乙组同学实验成功,能用于验证质量守恒定律.
你认为丙组同学对吗?为什么?
 查看习题详情和答案>>
查看习题详情和答案>>
(1)化学用语可准确简洁地记录、表达化学信息.请从Fe、Na、C、O 四种元素中选择适当的元素按要求填空:
①2个铁原子
2O3
2O3;
(2)“用微观的眼光看世界”是我们学习化学的重要思想方法,下面是某化学反应的微观模拟示意图,请据图回答:
①写出该反应的化学方程式:
②在E、G、L、M四种物质中,属于氧化物的是
③分析以上微观过程模拟图,你能总结出的一条规律是: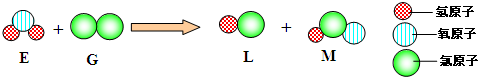
查看习题详情和答案>>
①2个铁原子
2Fe
2Fe
;②钠离子Na+
Na+
;③+3价的金属氧化物| +3 |
| Fe |
| +3 |
| Fe |
(2)“用微观的眼光看世界”是我们学习化学的重要思想方法,下面是某化学反应的微观模拟示意图,请据图回答:
①写出该反应的化学方程式:
H2O+Cl2=HCl+HClO
H2O+Cl2=HCl+HClO
;②在E、G、L、M四种物质中,属于氧化物的是
E
E
;③分析以上微观过程模拟图,你能总结出的一条规律是:
在化学反应前后原子的种类没有改变,数目没有增减
在化学反应前后原子的种类没有改变,数目没有增减
.
在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究.A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,他们都进行了规范的操作,准确的称量和细致地观察.

(1)A实验:白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡.结论是:质量不守恒;等锥形瓶冷却后,重新放在天平上称量,天平平衡.结论是:质量守恒.
你认为结论正确的是
白磷燃烧时的现象是
(2)B实验:乙组同学反应前调节天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向
(3)丙组同学认为C实验说明了质量守恒.请你从原子的角度说明为什么?
(4)由质量守恒定律可知,化学反应前后,一定不变的是
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质种类.
查看习题详情和答案>>

(1)A实验:白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡.结论是:质量不守恒;等锥形瓶冷却后,重新放在天平上称量,天平平衡.结论是:质量守恒.
你认为结论正确的是
后一种
后一种
(填“前一种”或“后一种”),导致另一种结论错误的原因是白磷燃烧放出的热量使气体受热膨胀,小气球胀大产生浮力,使得天平不平衡
白磷燃烧放出的热量使气体受热膨胀,小气球胀大产生浮力,使得天平不平衡
.白磷燃烧时的现象是
产生大量的白烟,放出热量
产生大量的白烟,放出热量
,该反应的化学方程式为4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
(2)B实验:乙组同学反应前调节天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向
右
右
偏转(填“左”或“右”).同学们得到的结论是“实验B说明质量不守恒”.老师引导同学们分析了原因.你认为B实验天平不平衡的原因是在敞口的容器中进行反应,生成的二氧化碳逸散到空气中
在敞口的容器中进行反应,生成的二氧化碳逸散到空气中
.若要得到正确结论,该实验应该在在密闭的容器中进行实验
在密闭的容器中进行实验
装置中进行.(3)丙组同学认为C实验说明了质量守恒.请你从原子的角度说明为什么?
反应前后原子的种类、数目、质量不变,因此生成物的质量也不会改变
反应前后原子的种类、数目、质量不变,因此生成物的质量也不会改变
.(4)由质量守恒定律可知,化学反应前后,一定不变的是
①②⑤⑥
①②⑤⑥
;(填序号,下同)一定改变的是③
③
;可能改变的是④
④
.①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质种类.
