网址:http://m.1010jiajiao.com/timu3_id_64578[举报]

(1)根据各图表示的结构特点,写出对应分子的化学式:
A____________;B____________;C____________;D____________。
(2)用以上图示表示下列物质的结构:
①H2O ②CH4 ③CO2 ④HClO
查看习题详情和答案>>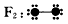 。以下四种图式各代表的分子是
。以下四种图式各代表的分子是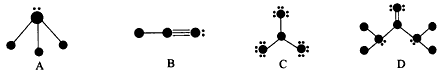
下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键,(示例:![]() )
)
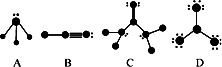
(1)根据各图表示的结构特点,写出对应分子的化学式:
A________;B________;C________;D________.
(2)用以上图示表示下列物质的结构:
①H2O ②CH4 ③CO2 ④HClO
太阳能电池的发展已经进入了第三代.第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.完成下列填空:
(1)亚铜离子(Cu+)基态时的电子排布式为______;
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为______ (用元素符号表示),用原子结构观点加以解释______;
(3)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成加合物,如BF3能与NH3反应生成BF3?NH3. BF3?NH3中B原子的杂化轨道类型为______,B与N之间形成______键;
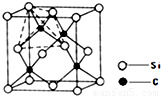
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构;在SiC中,每个C原子周围最近的C原子数目为______.
 查看习题详情和答案>>
查看习题详情和答案>>
①5种元素的原子半径按A、B、C、D、E的顺序从大到小排列;
②B、C均是地壳中含量较高的元素,B元素单质常温下遇浓硫酸钝化,C元素的单质及其氧化物的晶体结构成空间网状;
③C、D元素原子最外层电子数之和与A、B元素原子最外层电子数之和相同,而且E元素原子的最外层电子数为A、B、C、D四种元素原子最外层电子数之和的四分之一;
④E元素的一种氧化物能与水反应生成该元素最高价氧化物的水化物,同时生成E的另一种氧化物。
请回答以下问题:
(1)C元素原子结构示意图为___________;E的气态氢化物的电子式为___________;
(2)写出B的最高价氧化物的水化物在水中的电离方程式___________;
(3)D的某种氧化物中D元素的质量分数是50%,则该氧化物的性质有(填字母)___________;
A.可使溴水褪色 B.可使品红溶液褪色
C.通入氯化钡溶液,产生白色沉淀 D.溶于水,生成强酸
(4)A单质的浓溶液与一种有机物(C8H6O)反应能生成白色沉淀,写出有关反应的化学方程式___________________________________________ _________________________;
(5)E元素的气态氢化物可与热的氧化铜反应得到E的单质,每0.1 mol氧化铜完全反应时转移0.2 mol电子,写出有关反应的化学方程式________________________________________。
查看习题详情和答案>>