摘要: [提出假设]H2SO4溶液.MgSO4溶液.H2SO4溶液或MgSO4溶液 [实验验证] 实验步骤 实验现象 实验结论 (1)取该溶液少许于试管中.滴入紫色石蕊试液 (2)取该溶液少许于试管中.加入锌粒 (3)取该溶液少许于试管中.加入氧化铜 (d)取该溶液少许于试管中.加入氢氧化铜 (5)取该溶液少许于试管中.滴入碳酸钠溶液 紫色石蕊试液变红 锌粒表面有气泡产生 固体逐渐溶解.溶液变蓝 固体逐渐溶解.溶液变蓝 有气泡产生 该溶液是H2SO4溶液 或 实验步骤 实验现象 实验结论 取该溶液少许于试管中.滴入氢氧化钠溶液 出现白色沉淀 该溶液是MgSO4溶液 说明:本题属于开放性试题.只要答出一种且合理就可得满分.
网址:http://m.1010jiajiao.com/timu3_id_6359[举报]
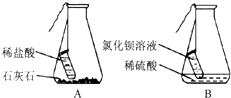 小刚和小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究.请填写以下探究过程中的空格:(A中的反应:2HCl+CaCO3=CaCl2+CO2↑+H2O;B中的反应:BaCl2+H2SO4=BaSO4↓+2HCl)
小刚和小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究.请填写以下探究过程中的空格:(A中的反应:2HCl+CaCO3=CaCl2+CO2↑+H2O;B中的反应:BaCl2+H2SO4=BaSO4↓+2HCl)[提出假设]化学反应中,反应物与生成物质量
相等
相等
.(“相等”或者“不相等”)[确定研究方法]分析推理、查阅资料、实验探究.
[设计并进行实验]小刚设计的实验装置和选用药品如A图所示,小洁设计的实验装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
[实验结论]小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等.小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等.
你认为
小洁
小洁
的结论正确,请谈谈导致另一种结论错误的原因该实验没有在密闭的容器中进行,生成的二氧化碳逸出了
该实验没有在密闭的容器中进行,生成的二氧化碳逸出了
[结论分析]请从原子的角度,简要分析你认为正确的结论
反应前后原子的种类,数目和质量都没有改变
反应前后原子的种类,数目和质量都没有改变
[查阅资料]小刚和小洁通过查阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确、缜密的研究,并做出了科学结论.
[交流表达]请简要谈一下,你认为这条科学结论有什么重大意义?
该科学结论对于定量认识化学反应,合理进行化工生产有重要作用.
该科学结论对于定量认识化学反应,合理进行化工生产有重要作用.
.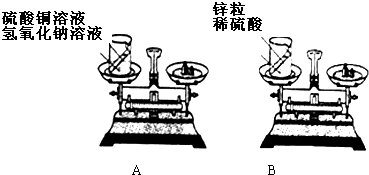 (2009?金山区一模)为研究物质发生化学变化的前后总质量是否发生改变,小刘、小李按以下步骤进行探究:
(2009?金山区一模)为研究物质发生化学变化的前后总质量是否发生改变,小刘、小李按以下步骤进行探究:(1)提出假设:物质发生化学变化前后总质量不变.
(2)设计并实验:小刘设计的实验装置和选用药品如A所示,小李设计的实验装置和选用药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
①小刘实验的化学反应方程式是
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
,反应观察到的现象是烧杯中有蓝色沉淀生成,反应后物质的质量不变
烧杯中有蓝色沉淀生成,反应后物质的质量不变
;小李实验的化学反应方程式是Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
;②实验结论:小刘认为:在化学反应中,生成物的总质量与反应物的总质量相等;小李认为:在化学反应中,生成物的总质量与反应物的总质量不相等.
③你认为
小刘
小刘
的结论正确,导致另一个实验结论错误的原因是小李未考虑生成的气体逸散到空气中的质量
小李未考虑生成的气体逸散到空气中的质量
. 23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.
23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.(1)查阅资料:①SO2常温下是一种无色气体,易溶于水;②酸能使蓝色石蕊试纸变成红色;③SO2有毒.
(2)提出假设:SO2能与H2O反应生成酸.
(3)实验探究:设计如右图所示装置进行实验.
①实验过程中,A装置内蓝色石蕊试纸的颜色始终没有变化.A装置的作用是
证明SO2不能使蓝色石蕊试纸变色
.②在通入SO2之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,此步操作的目的是
证明水不能使蓝色石蕊试纸变色
.当有SO2通过时发现湿润的蓝色石蕊试纸变红,此现象说明
SO2与水反应生成酸
,此过程中反应的化学方程式为
SO2+H2O=H2SO3
.(4)结论:原假设成立.
(5)反思与评价:该实验方案中,有一个明显的疏漏,请你帮他们指出不足之处
尾气没有处理
.(6)拓展探究:该研究性学习小组取刚降到硫酸厂(生产过程中产生SO2)附近的雨水进行测定,每隔几分钟测一次pH,其数据如下表所示:

分析上述数据的变化,你可得出的结论是
随着时间的变化,雨水的酸性逐渐增强
;针对此结论,你猜测其中的原因为
H2SO3与空气中的O2反应生成了H2SO4
.结合大理石雕像受到酸雨腐蚀的事实,你认为碳酸、硫酸、亚硫酸(H2SO3)酸性由强到弱的顺序是
H2SO4>H2SO3>H2CO3
.23、人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究.
(1)以下工具的制作过程中没有发生化学变化的是(
A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序
A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与
(3)金属区别于非金属的主要物理性质是,金属具有
(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3△2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是
(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由
b.在合成该超导材料的同时还生成-种产物,该物质是
金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有
(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
[实验现象]
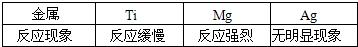
[实验结论]原假设中
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验
结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).
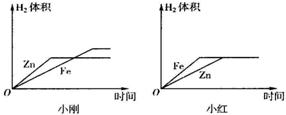
两个图象中存在有错误的是
图象不同的原因是
由该实验可以得到的结论:
①金属与酸反应的速率与
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与
(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有
(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
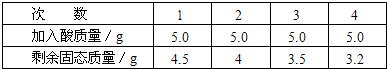
试求:①合金中铜的质量分数
查看习题详情和答案>>
(1)以下工具的制作过程中没有发生化学变化的是(
A
)A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序
B.A.C
(填序号).A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与
金属活动性
有关,那么金属钾的制得应排在C
之后.(3)金属区别于非金属的主要物理性质是,金属具有
金属光泽
,金属区别于非金属的主要化学特征是良好的传热导电性
.在化学变化中金属原子通常表现为延展性易失去电子
.(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3△2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:
2CuO+2C═2Cu+CO2↑
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
不能,在化学变化过程中元素种类不可能发生改变
.②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是
铜锌合金
,炼出它的化学方程式为ZnCO3═ZnO+CO2↑
、2ZnO+C═2Zn+CO2↑
、2Cu2O+C═4Cu+CO2↑
.(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:
Fe+CuSO4═Cu+FeSO4
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由
四
种元素组成的,YmOn的化学式是:Y2O3
b.在合成该超导材料的同时还生成-种产物,该物质是
CO2
(写化学式).金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有
恨铁不成钢
,知道“百炼成钢”是指铁在高温条件下反复敲打发生的反应是:C+O2═CO2
,从而了解钢与铁的机械性能不同是因为两者含碳量不等
.(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
除去氧化膜利于直接反应
.[实验现象]

[实验结论]原假设中
a
不正确,理由是镁反应速率比钛快
.[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?
否
,请说明理由反应速率与反应物浓度有关
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验
结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).

两个图象中存在有错误的是
小红
的图象,判断错误的理由是图象中Fe与Zn标反了,Zn的反应速率较Fe快
,图象不同的原因是
小刚取的金属量较少,金属反应完,而小红取的酸量较少,酸完全反应完
.由该实验可以得到的结论:
①金属与酸反应的速率与
金属活动性
有关.②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与
相对原子质量
有关.(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有
Ag、Zn(NO3)2
,肯定滤液中有Fe(NO3)2
.(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:

试求:①合金中铜的质量分数
64%
.②合金中另一金属为何种金属.另一种金属为锌
. 室验室开放日,小明同学来到实验室,看到实验桌上摆放着一瓶标签破损的无色溶液,可能是什么物质,他大胆猜想并设计实验进行验证.
室验室开放日,小明同学来到实验室,看到实验桌上摆放着一瓶标签破损的无色溶液,可能是什么物质,他大胆猜想并设计实验进行验证.[发现问题]当把某种固体与无色溶液混合时即产生气泡.
[查阅资料、提出假设]①若固体是石灰石,无色溶液可能是
稀盐酸
稀盐酸
.(只写一种假设,下同)反应方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
若固体是锌粒,无色溶液可能是
稀硫酸
稀硫酸
.(要求与上面假设不同)反应方程式是Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
若固体是二氧化锰,无色溶液可能是
过氧化氢溶液
过氧化氢溶液
.(要求与上面假设不同)反应方程式是2H2O2═2H2O+O2↑
2H2O2═2H2O+O2↑
[设计实验]小明根据假设,向盛有少许石灰石的试管中加入适量的该无色溶液,有气泡;用如图收集一瓶产生的气体;则气体由
b
b
(填a或b)端进入.检验气体:向瓶中注入澄清石灰水
澄清石灰水
振荡.[实验现象]
出现白色浑浊
出现白色浑浊
.[实验结论]此气体是二氧化碳,该无色液体可能是稀盐酸.