网址:http://m.1010jiajiao.com/timu3_id_62909[举报]

(1)实验时,先将B装置下移,使碳酸钙和稀硝酸接触产生气体,当C处产生白色沉淀时,立即将B装置上提,使之与硝酸分离。该组学生设计此操作的目的是___________________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为__________________________。装置E中开始出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是__________________,一段时间后,C中白色沉淀溶解,其原因是_________________________________________。
(3)装置D的作用_______________________________________________________。
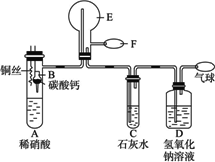
查看习题详情和答案>>为了验证铜和稀硝酸反应产生了NO,某学生实验小组设计了一个实验,其装置如下图.B为一个用金属丝固定的干燥管,内装块状碳酸钙固体,E为一个空的蒸馏烧瓶,F是用于鼓入空气的双连打气球.
(1)实验时,先将B装置下移,使碳酸钙和稀硝酸接触产生气体,当C处产生白色沉淀时,立即将B装置上提,使之与硝酸分离.该组学生设计此操作的目的是_________________.
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为________.装置E中开始出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是__________,一段时间后,C中白色沉淀溶解,其原因是____________.
(3)装置D的作用____________.
某课外活动小组为了验证铜与稀硝酸反应产生的气体是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹,F是装有一半空气的注射器。

请回答有关问题:
(1)设计装置A的目的是 ,如何判断已完成该目的__________________
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是 ;B中反应的离子方程式为: 。
(3)装置E和F的作用是 ;为实现此作用,其操作方法是 。
(4)装置D的作用是 。
查看习题详情和答案>>1. 某课外活动小组为了验证铜与稀硝酸反应产生的气体是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹,F是装有一半空气的注射器。
2.
3. 请回答有关问题:
4. (1)设计装置A的目的是 ,如何判断已完成该目的__________________
5. (2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是 ;B中反应的离子方程式为: 。
6. (3)装置E和F的作用是 ;为实现此作用,其操作方法是 。
7. (4)装置D的作用是 。
查看习题详情和答案>>
(13分)为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。
(1)实验时,第一步实验操作为:将装有CaCO3干燥管下移与稀硝酸反应生成CO2,该操作作用为 。反应的化学方程式为 。
从装置的设计看,确定E中空气已被赶尽的实验现象是
。
(2)第二步,提起干燥管B, 将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明?
。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是 。
(4)装置D的作用是 。
(5)将一定量铜与足量稀硝酸充分反应,可以得到4.48L NO气体(气体体积在标准状况下测定),若反应后溶液体积为100mL,则所得溶液中Cu2+的物质的量浓度是
查看习题详情和答案>>