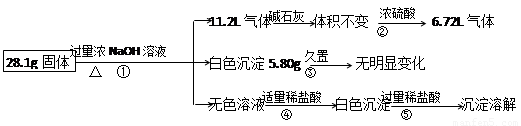网址:http://m.1010jiajiao.com/timu3_id_62783[举报]
(11分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
请回答
(1)混合物中是否存在FeCl2_________(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。
(3)写出反应⑤的离子反应方程式;___________________________________。
(4)请根据图中数据分析,原固体混合物的成分为_____________________(写化学式)。
查看习题详情和答案>>
(12分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):回答下列问题:
(1)混合物中是否存在FeCl2 ___ (填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4 ___(填“是”或“否”),你的判断依据是 。
(3)写出反应⑤的离子方程式: 。
(4)请根据计算结果判断混合物中是否含有AlCl3 ___(填“是”或“否”),你的判断依据是 。
查看习题详情和答案>>
(12分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):回答下列问题:
(1)混合物中是否存在FeCl2 ___ (填“是”或“ 否”);
否”);
(2)混合物中 是否存在(NH4)2SO4 ___(填“是”或“否”),你的判断依据是 。
是否存在(NH4)2SO4 ___(填“是”或“否”),你的判断依据是 。
(3)写出反应⑤的离子方程式: 。
(4)请根据计算结果判断混合物中是否含有AlCl3 ___(填“是”或“否”),你的判断依据是 。
(11分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):





 请回答
请回答 (1)混合物中是否存在FeCl2_________(填“是”或“否”);
(1)混合物中是否存在FeCl2_________(填“是”或“否”); (2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。
(2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。 (3)写出反应⑤的离子反应方程式;___________________________________。
(3)写出反应⑤的离子反应方程式;___________________________________。 (4)请根据图中数据分析,原固体混合物的成分为
(4)请根据图中数据分析,原固体混合物的成分为 _____________________(写化学式)。
_____________________(写化学式)。