摘要:16.已知:离子化合物M中金属元素的质量分数为35.4%.M在汽车安全气囊中有重要的作用.常温下G为淡黄色固体.H为一种常见的液体.A.B.C.X为单质.其中A.C.X为气体.A.X均为空气中的主要成分.I.J为常见的工业原料. 相关转化关系如图所示: (1)实验室中物质I应如何保存 (2)写出D与X反应的化学方程式 (3)G.F均能氧化SO2 .若前一反应仅生成一种盐.后一反应生成两种氧化物.试写出相应化学方程式 . (4)常温下M受撞击时可分解.13gM完全分解为A和B时.放出a kJ的热量.写出M分解的热化学方程式 (5)M是一种易溶于水的盐.其水溶液显弱碱性.用离子方程式解释原因 酸R与J反应生成M和H.常温下.将pH=4的R溶液与pH=10的J溶液等体积混合.所得溶液中各离子浓度大小关系为 (已知:酸R的酸性与醋酸相近)
网址:http://m.1010jiajiao.com/timu3_id_62358[举报]
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.请回答下列问题:
(1)B、C、D三种元素的电负性由大到小的顺序是
O>N>C
O>N>C
(填元素符号).(2)在A元素与上述其他元素形成的分子中,其中心原子为sp3杂化的为
CH4、H2O
CH4、H2O
.(写出2种即可)(3)与C同族且位于第四周期元素所形成气态氢化物的电子式为


极性
极性
(填“极性”或“非极性”)分子.(4)F的基态原子核外电子排布式是
1s22s22p63s23p63d24s2
1s22s22p63s23p63d24s2
.在F的单质晶体中,F原子的堆积方式是六方最密堆积
六方最密堆积
,F原子的配位数是12
12
.(5)E原子的第一电离能比同周期后面相邻元素的第一电离能
大
大
(填“大”或“小”).E与D形成化合物的熔点高,其原因是离子半径小,离子所带电荷多,晶格能大
离子半径小,离子所带电荷多,晶格能大
.(6)氢气是理想的清洁能源,X元素与镧(La)元素的合金可作储氢材料,该合金的晶胞如图所示,晶胞中心有一个X原子,其他X原子都在晶胞面上,则该晶体的化学式为
Ni5La
Ni5La
.已知该晶体的密度为d g?cm-3,其摩尔质量为M g?mol-1,则该晶胞的边长是| 3 |
| ||
| 3 |
| ||
已知:A为一种矿石的主要成分,呈淡黄色,是工业生产j的原料,是化学工业生产中一种重要的酸.B、C、H、I均为短周期元素组成的非金属单质,K为常见的金属单质.X分子是含有非极性键的极性分子,其水溶液为一种常见的无色医用消毒液.F为常见的红棕色防锈油漆颜料的主要成分.O是有机物,而且是一种常见的含氮量很高的氮肥,且反应⑦中L与M的物质的量之比为1:2,A、E、J、N中含有同一种元素.下图转化关系中,有多个反应为工业生产中的反应,根据下图回答下列问题.
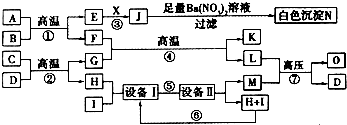
(1)工业生产中反应①发生的设备名称是______,X的化学式为______,L的结构式为______.
(2)A与B反应的化学反应方程式为______.
(3)C有多种同素异形体,其中一种可以导电.反应②的化学方程式为______.
(4)考虑到综合经济效益,工业生产M时,可采取的措施很多,下述措施中不宜采用的有______ (填字母序号)
a.使用催化剂 b.适当降低温度 C.选择合适的温度 d.适度增大压强 e.及时分离出产物 f提高原料的利用率
g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 i.工厂地址可选择在盛产天然气的地区
(5)L与D反应可以生成一种常见的不稳定的二元弱酸,有机物O可以看作是此二元弱酸的衍生物,写出反应⑦的化学方程式______.
查看习题详情和答案>>
(8分)已知:L、M、Q、R、T五种短周期元素,有如下信息:
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
最高正价或最低负价 | +2 | +3 | +2 | +6、-2 | -2 |
根据上述信息回答下列问题:
⑴M元素在周期表的位置为 周期 族。
⑵L离子的结构示意图是 ,L元素与T元素形成的化合物的化学键为 (填“离子键”、“共价键”)。
⑶T元素形成的含有18电子的无机共价化合物的化学式为 。
⑷L、M、Q三种元素中,金属性最强的是 。写出能说明R与T元素非金属性强弱的一个化学方程式 。
查看习题详情和答案>>
已知:A为一种矿石的主要成分,呈淡黄色,是工业生产j的原料,是化学工业生产中一种重要的酸.B、C、H、I均为短周期元素组成的非金属单质,K为常见的金属单质.X分子是含有非极性键的极性分子,其水溶液为一种常见的无色医用消毒液.F为常见的红棕色防锈油漆颜料的主要成分.O是有机物,而且是一种常见的含氮量很高的氮肥,且反应⑦中L与M的物质的量之比为1:2,A、E、J、N中含有同一种元素.下图转化关系中,有多个反应为工业生产中的反应,根据下图回答下列问题.
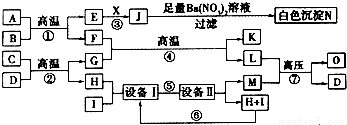
(1)工业生产中反应①发生的设备名称是 ,X的化学式为 ,L的结构式为 .
(2)A与B反应的化学反应方程式为 .
(3)C有多种同素异形体,其中一种可以导电.反应②的化学方程式为 .
(4)考虑到综合经济效益,工业生产M时,可采取的措施很多,下述措施中不宜采用的有 (填字母序号)
a.使用催化剂 b.适当降低温度 C.选择合适的温度 d.适度增大压强 e.及时分离出产物 f提高原料的利用率
g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 i.工厂地址可选择在盛产天然气的地区
(5)L与D反应可以生成一种常见的不稳定的二元弱酸,有机物O可以看作是此二元弱酸的衍生物,写出反应⑦的化学方程式 . 查看习题详情和答案>>

(1)工业生产中反应①发生的设备名称是 ,X的化学式为 ,L的结构式为 .
(2)A与B反应的化学反应方程式为 .
(3)C有多种同素异形体,其中一种可以导电.反应②的化学方程式为 .
(4)考虑到综合经济效益,工业生产M时,可采取的措施很多,下述措施中不宜采用的有 (填字母序号)
a.使用催化剂 b.适当降低温度 C.选择合适的温度 d.适度增大压强 e.及时分离出产物 f提高原料的利用率
g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 i.工厂地址可选择在盛产天然气的地区
(5)L与D反应可以生成一种常见的不稳定的二元弱酸,有机物O可以看作是此二元弱酸的衍生物,写出反应⑦的化学方程式 . 查看习题详情和答案>>
已知化合物A与B组成元素相同,在常温下均呈液态;D与E都为金属单质,且D、E与甲的浓溶液在常温作用都无明显现象,加热时有大量红棕色气体产生.E与D的氧化物的反应可用于焊接钢轨.
(1)A的结构式为
(2)写出过量D与甲稀溶液反应的离子方程式:
(3)以D、E为电极,NaOH溶液为电解质溶液可以组成原电池,原电池负极的电极反应式为
(4)含有D、E元素的一种新型无机高分子材料高效净水剂[ED(OH)4Cl2]m与过量浓盐酸溶液可以反应,其反应的化学方程式为
查看习题详情和答案>>
(1)A的结构式为
H-O-O-H
H-O-O-H
,说出A在医疗中的一种重要作用杀菌消毒
杀菌消毒
.(2)写出过量D与甲稀溶液反应的离子方程式:
3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
;(3)以D、E为电极,NaOH溶液为电解质溶液可以组成原电池,原电池负极的电极反应式为
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.现利用此装置电解CuSO4溶液,电解一段时间后,阴阳两极产生的气体在标准状况下都是2.24L.请写出阳极的电极反应式4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
;若电解前CuSO4溶液的体积为200mL,则其物质的量浓度是0.5mol/L
0.5mol/L
;(4)含有D、E元素的一种新型无机高分子材料高效净水剂[ED(OH)4Cl2]m与过量浓盐酸溶液可以反应,其反应的化学方程式为
:[AlFe(OH)4Cl2]m+4mHCl=mAlCl3+mFeCl3+4mH2O
:[AlFe(OH)4Cl2]m+4mHCl=mAlCl3+mFeCl3+4mH2O
.