网址:http://m.1010jiajiao.com/timu3_id_62046[举报]
(12分)“问题胶囊”事件引发了各方关注和热议,国际食品包装协会秘书长董金狮教授说:“工业明胶中重金属铬的毒性远高于三聚氰胺”。铬是严重的致癌物质,绝不允许含铬废水随意排放。请回答下列问题: 
(1)三聚氰胺中N原子的杂化方式是 .
(2)酸性溶液中过氧化氢能使Cr2072-生成蓝色的过氧化铬(CrO5,分子结构为 ),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为 , 请写出反应的离子方程式: 。
),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为 , 请写出反应的离子方程式: 。
(3)一种治理含Cr2072-酸性工业废水的方法是向废水中加入适量的食盐,用铁作电极进行电解,Cr2072-被还原为Cr3+,然后生成Cr(OH)3沉淀除去,以达到排放标准。
①加适量食盐的目的是 ,与Cr(OH)3沉淀同时生成的沉淀还可能有 。
②已知电解后溶液中c(Fe3+)为4.Ox10-13mol.L-1,则溶液中c(Cr3+)浓度为 。
(已知KsP[Fe(OH)3]=4.0×10-38; Ksp[Cr(OH)3]=6.0×10-31)
(12分)“问题胶囊”事件引发了各方关注和热议,国际食品包装协会秘书长董金狮教授说:“工业明胶中重金属铬的毒性远高于三聚氰胺”。铬是严重的致癌物质,绝不允许含铬废水随意排放。请回答下列问题:

(1)三聚氰胺中N原子的杂化方式是 .
(2)酸性溶液中过氧化氢能使Cr2072-生成蓝色的过氧化铬(CrO5,分子结构为  ),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为
, 请写出反应的离子方程式:
。
),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为
, 请写出反应的离子方程式:
。
(3)一种治理含Cr2072-酸性工业废水的方法是向废水中加入适量的食盐,用铁作电极进行电解,Cr2072-被还原为Cr3+,然后生成Cr(OH)3沉淀除去,以达到排放标准。
①加适量食盐的目的是 ,与Cr(OH)3沉淀同时生成的沉淀还可能有 。
②已知电解后溶液中c(Fe3+)为4.Ox10-13mol.L-1,则溶液中c(Cr3+)浓度为 。
(已知KsP[Fe(OH)3]=4.0×10-38; Ksp[Cr(OH)3]=6.0×10-31)
查看习题详情和答案>>

(1)三聚氰胺中N原子的杂化方式是 .
(2)酸性溶液中过氧化氢能使Cr2072-生成蓝色的过氧化铬(CrO5,分子结构为
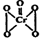 ),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为 , 请写出反应的离子方程式: 。
),该反应可用来检验Cr2072-的存在。过氧化铬中铬元素的化合价为 , 请写出反应的离子方程式: 。(3)一种治理含Cr2072-酸性工业废水的方法是向废水中加入适量的食盐,用铁作电极进行电解,Cr2072-被还原为Cr3+,然后生成Cr(OH)3沉淀除去,以达到排放标准。
①加适量食盐的目的是 ,与Cr(OH)3沉淀同时生成的沉淀还可能有 。
②已知电解后溶液中c(Fe3+)为4.Ox10-13mol.L-1,则溶液中c(Cr3+)浓度为 。
(已知KsP[Fe(OH)3]=4.0×10-38; Ksp[Cr(OH)3]=6.0×10-31)