摘要:22.把l mol CO2和3mol H2通入l L的密闭容器中.在某温度下发生反应: CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H=–49.0 kJ·mol-1 测得CO2和CH3OH的浓度随时间变化如下图所示.下列说法正确的是 A.3min时.v正=v逆 B.0-10 min内.氢气的平均反应速率为0.225 mol·L-1·min-1 C.该温度下.反应的平衡常数K=5.3 mol-2·L2 D.若升高温度.CO2的平衡转化率大于75%
网址:http://m.1010jiajiao.com/timu3_id_61272[举报]
 把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是( )
| A、3min时,v正=v逆 | B、0~10 min内,氢气的平均反应速率为0.225 mol?L-1?min-1 | C、该温度下,反应的平衡常数K=5.3 mol-2?L2 | D、若升高温度,CO2的平衡转化率大于75% |
低碳经济是以低能耗、低污染、低排放为基础的经济模式,低碳循环正成为科学家研究的主要课题.
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:
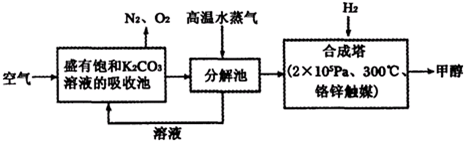
(1)向分解池中通入高温水蒸气的作用是 .
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为 .
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正 v逆值(填“>”、“<”或“=”).
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是 .
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.
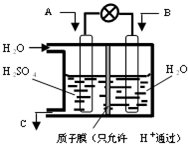
(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为 .
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为 .
查看习题详情和答案>>
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:

(1)向分解池中通入高温水蒸气的作用是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.2 | 0.4 |
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.

(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为
(Ⅰ)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+1/2O2 (g)=CO (g)+2H2(g)△H1=-35.6kJ?molˉ1
试判断常温下,上述反应能否自发进行______(填“能”或“否”),有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2 (g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?molˉ1
③CH4(g)+CO2 (g)=2CO (g)+2H2(g)△H3=247.3kJ?molˉ1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O (g)=CO (g)+3H2(g)△H=______kJ?molˉ1
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:

此条件下,该反应达到化学平衡时,氮气的浓度为______.
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式______.
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好______.
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10ˉ3mol?Lˉ1,则pC=-lg(1×10ˉ3)=3.某温度下,H2CO3溶液的pC-pH关系如图.
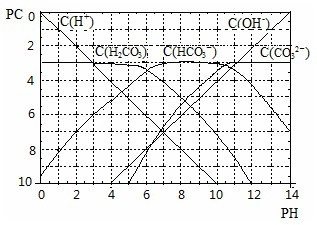
请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为______;
(2)求此温度下H2CO3

H++HCO3ˉ 的电离平衡常数______;
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?Lˉ1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3ˉ

H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液______.
查看习题详情和答案>>
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+1/2O2 (g)=CO (g)+2H2(g)△H1=-35.6kJ?molˉ1
试判断常温下,上述反应能否自发进行______(填“能”或“否”),有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2 (g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?molˉ1
③CH4(g)+CO2 (g)=2CO (g)+2H2(g)△H3=247.3kJ?molˉ1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O (g)=CO (g)+3H2(g)△H=______kJ?molˉ1
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/( mol?Lˉ1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

此条件下,该反应达到化学平衡时,氮气的浓度为______.
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式______.
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好______.
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10ˉ3mol?Lˉ1,则pC=-lg(1×10ˉ3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为______;
(2)求此温度下H2CO3

H++HCO3ˉ 的电离平衡常数______;
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?Lˉ1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3ˉ

H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液______.
(2011?嘉兴模拟)(Ⅰ)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+
O2(g)=CO(g)+2H2(g)△H1=-35.6kJ?mol-1
试判断常温下,上述反应能否自发进行
②CH4(g)+2O2(g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?mol-1
③CH4(g)+CO2(g)=2CO(g)+2H2(g)△H3=247.3kJ?mol-1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
 此条件下,该反应达到化学平衡时,氮气的浓度为
此条件下,该反应达到化学平衡时,氮气的浓度为
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol?L-1,则pC=-lg(1×10-3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为
(2)求此温度下H2CO3?H++HCO3-的电离平衡常数
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3-?H++CO32-移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液
查看习题详情和答案>>
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+
| 1 |
| 2 |
试判断常温下,上述反应能否自发进行
能
能
(填“能”或“否”),有研究认为甲烷部分氧化的机理为:②CH4(g)+2O2(g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?mol-1
③CH4(g)+CO2(g)=2CO(g)+2H2(g)△H3=247.3kJ?mol-1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=
250.3
250.3
kJ?mol-1(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol?L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 此条件下,该反应达到化学平衡时,氮气的浓度为
此条件下,该反应达到化学平衡时,氮气的浓度为0.4mol/L
0.4mol/L
.(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式
N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
.(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好
A
A
.A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol?L-1,则pC=-lg(1×10-3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为
H+、HCO3-
H+、HCO3-
;(2)求此温度下H2CO3?H++HCO3-的电离平衡常数
10-6mol/L
10-6mol/L
;(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3-?H++CO32-移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液
能
能
.
(Ⅰ)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+1/2O2 (g)=CO (g)+2H2(g)△H1=-35.6kJ?molˉ1
试判断常温下,上述反应能否自发进行 (填“能”或“否”),有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2 (g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?molˉ1
③CH4(g)+CO2 (g)=2CO (g)+2H2(g)△H3=247.3kJ?molˉ1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O (g)=CO (g)+3H2(g)△H= kJ?molˉ1
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
此条件下,该反应达到化学平衡时,氮气的浓度为 .
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式 .
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好 .
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10ˉ3mol?Lˉ1,则pC=-lg(1×10ˉ3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 ;
(2)求此温度下H2CO3 H++HCO3ˉ 的电离平衡常数 ;
H++HCO3ˉ 的电离平衡常数 ;
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?Lˉ1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3ˉ H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 .
H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+1/2O2 (g)=CO (g)+2H2(g)△H1=-35.6kJ?molˉ1
试判断常温下,上述反应能否自发进行 (填“能”或“否”),有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2 (g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?molˉ1
③CH4(g)+CO2 (g)=2CO (g)+2H2(g)△H3=247.3kJ?molˉ1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O (g)=CO (g)+3H2(g)△H= kJ?molˉ1
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/ | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式 .
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好 .
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10ˉ3mol?Lˉ1,则pC=-lg(1×10ˉ3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 ;
(2)求此温度下H2CO3
 H++HCO3ˉ 的电离平衡常数 ;
H++HCO3ˉ 的电离平衡常数 ;(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?Lˉ1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3ˉ
 H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 .
H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 . 查看习题详情和答案>>
查看习题详情和答案>>