摘要:12.做溶解.过滤.蒸发实验均要用到的一种仪器是 ( ) A.试管 B.烧杯 C.酒精灯 D.玻璃棒
网址:http://m.1010jiajiao.com/timu3_id_6104[举报]
某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是 (填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是 .
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL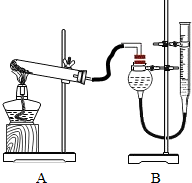 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
(3)上述实验中的“待测数据”指 .
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a. ;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+
c.K2MnO4+Cl2=2KCl+MnO2+O2↑ 查看习题详情和答案>>
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是
(2)步骤、中研磨固体所用仪器的名称是
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL
 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | 0.5g CuO | |
| ⑥ | 1.2g | 0.5g MnO2 |
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+
c.K2MnO4+Cl2=2KCl+MnO2+O2↑ 查看习题详情和答案>>
某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是______(填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是______.
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
(3)上述实验中的“待测数据”指______.
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.______;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+______
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
 查看习题详情和答案>>
查看习题详情和答案>>
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是______(填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是______.
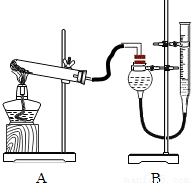
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | 0.5g CuO | |
| ⑥ | 1.2g | 0.5g MnO2 |
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.______;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+______
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
 查看习题详情和答案>>
查看习题详情和答案>>
某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是______(填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是______.
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL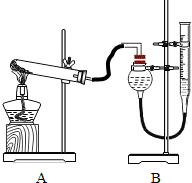 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
(3)上述实验中的“待测数据”指______.
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.______;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+______
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
查看习题详情和答案>>
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是______(填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是______.
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL
 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | 0.5gCuO | |
| ⑥ | 1.2g | 0.5gMnO2 |
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.______;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+______
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
化学实验室的开放日,老师安排兴趣小组的同学们作如下的实验研究:
(1)第一小组的同学将失去标签的两瓶无色溶液(分别为NaCl和Na2CO3)区分开来,为了区别无色溶液,甲、乙、丙、丁四位同学分别选择下列物质进行实验.你认为其中合理的试剂是
甲:稀盐酸 乙:硝酸银 丙:澄清石灰水 丁:蓝色石蕊试纸
(2)第二小组的同学为除去NaCl溶液中的少量 Na2CO3,设计了如下实验:

①写出沉淀A的化学式
②甲同学认为:蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和
③乙同学认为:加入过量CaCl2溶液不妥,其原因为
(3)第三小组同学了解到“三酸两碱”是重要的化工原料.实验室桌面上的五个试剂瓶内(如下图)分别装有属于工业上“三酸两碱”中的“三种浓酸”和“两碱固体”.
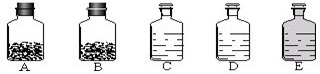
某同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是
②分别打开C、D瓶的瓶塞,观察到
(4)第四小组同学称取市售的纯碱样品12g加入适量水,再加入适量CaCl2溶液(所含杂质均可溶于水,且不参加反应),搅拌、过滤、洗涤、干燥后称得固体质量为10.0g:①求该样品中纯碱的质量分数;②若加入水和CaCl2溶液总质量为100g,则生成物溶液中溶质NaCl的质量分数为多少?
[计算过程].
查看习题详情和答案>>
(1)第一小组的同学将失去标签的两瓶无色溶液(分别为NaCl和Na2CO3)区分开来,为了区别无色溶液,甲、乙、丙、丁四位同学分别选择下列物质进行实验.你认为其中合理的试剂是
甲、丙
甲、丙
(填写序号)甲:稀盐酸 乙:硝酸银 丙:澄清石灰水 丁:蓝色石蕊试纸
(2)第二小组的同学为除去NaCl溶液中的少量 Na2CO3,设计了如下实验:

①写出沉淀A的化学式
CaCO3
CaCO3
;②甲同学认为:蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和
玻璃棒
玻璃棒
;③乙同学认为:加入过量CaCl2溶液不妥,其原因为
加入过量的氯化钙溶液会使氯化钠溶液中混有氯化钙溶液不纯
加入过量的氯化钙溶液会使氯化钠溶液中混有氯化钙溶液不纯
.(3)第三小组同学了解到“三酸两碱”是重要的化工原料.实验室桌面上的五个试剂瓶内(如下图)分别装有属于工业上“三酸两碱”中的“三种浓酸”和“两碱固体”.

某同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是
浓硝酸
浓硝酸
(填名称);②分别打开C、D瓶的瓶塞,观察到
C瓶的瓶口冒白雾
C瓶的瓶口冒白雾
,说明C瓶内的是浓盐酸,D瓶内的是浓硫酸.(4)第四小组同学称取市售的纯碱样品12g加入适量水,再加入适量CaCl2溶液(所含杂质均可溶于水,且不参加反应),搅拌、过滤、洗涤、干燥后称得固体质量为10.0g:①求该样品中纯碱的质量分数;②若加入水和CaCl2溶液总质量为100g,则生成物溶液中溶质NaCl的质量分数为多少?
[计算过程].