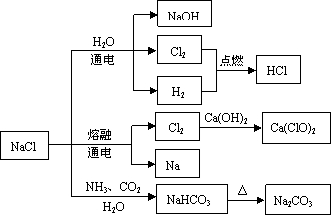
摘要:25.4g NaHCO3与AgNO3的混合物加热到500℃.待不再放出气体为止.冷却.加入足量的稀硝酸然后小心将溶液蒸干.的无水盐25.5g.在原测混合物中AgNO3的质量是 ( ) 8.4g (D) 9.2g [简析]此题的巧妙之处也在终端思维.最终的变化是把 NaHCO3→NaNO3 Dm 84g 85g 1g 现增加25.5g-25.4g=0.1g 所以原混合物中NaHCO3占8.4g.AgNO3则占17g.选(A).
网址:http://m.1010jiajiao.com/timu3_id_60988[举报]
NaCl是一种化工原料,可以制备一系列物质(见图),下列说法正确的是( )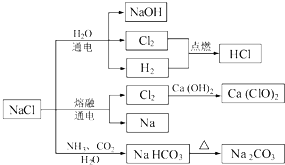

| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 | B、石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | C、电解熔融NaCl可制得金属钠 | D、图4所示转化反应都是氧化还原反应 |
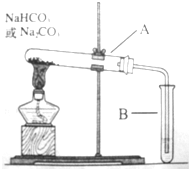 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.
某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成.
(1)设计实验:①利用如图装 置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
(2)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(3)某同学在探究NaHCO3的热稳定性时,称取了8.4g NaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
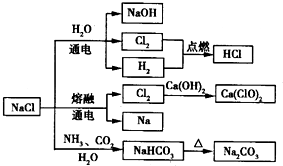 (2011?江苏)NaCl是一种化工原料,可以制备一系列物质.下列说法正确的是( )
(2011?江苏)NaCl是一种化工原料,可以制备一系列物质.下列说法正确的是( )