摘要: ⑴ 原子数目和电子总数相同的微粒互称等电子体.等电子体具有相似的结构特征.试写出短周期元素形成的含有14个电子的分子的化学式: .其中 和 互为等电子体.CO分子的电子式为 . ⑵ CH3CHO分子中.-CH3中的碳原子采用 杂化方式.-CHO中的碳原子采取 杂化方式. ⑶ 2007年诺贝尔化学奖获得者Gerhard Ertl利用光电子能谱证实:洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子.右图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子.灰色球代表铁原子).则在图示状况下.铁颗粒表面上N/Fe原子数比值的最大值为 .
网址:http://m.1010jiajiao.com/timu3_id_60216[举报]
A、B、C、D、E为短周期元素,其原子序数依次增大.其中,A元素原子半径最小;B元素原子的电子总数与最外层电子数之比为3:2;C元素最高价氧化物对应水化物与其氢化物反应生成一种盐甲.A、E同主族,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.请回答:
(1)写出B元素在周期表中的位置______,C单质的电子式是______.
(2)常温下,甲的水溶液pH______7(填“>、<或=”),其原因是(用离子方程式表示)______.
(3)B、D、E组成的化合物丙,其水溶液pH大于7.则丙的组成可能是______(填化学式).
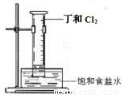
(4)A和B组成化合物丁,其相对分子质量为16.将如图装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状液滴生成等现象.油状液滴的成分是______(填化学式).
(5)A、D、E组成的化合物乙与氯化亚铁溶液反应可用于制备Fe3O4.制备流程如下:
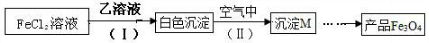
①写出步骤(Ⅰ)反应的离子方程式______.
②步骤(Ⅱ)的反应方程式是4Fe(OH)2+2H2O+O2═4Fe(OH)3,制备时应控制“一定量空气”的目的是______.
③由沉淀M获得Fe3O4的过程中发生的反应为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出B元素在周期表中的位置______,C单质的电子式是______.
(2)常温下,甲的水溶液pH______7(填“>、<或=”),其原因是(用离子方程式表示)______.
(3)B、D、E组成的化合物丙,其水溶液pH大于7.则丙的组成可能是______(填化学式).
(4)A和B组成化合物丁,其相对分子质量为16.将如图装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状液滴生成等现象.油状液滴的成分是______(填化学式).
(5)A、D、E组成的化合物乙与氯化亚铁溶液反应可用于制备Fe3O4.制备流程如下:

①写出步骤(Ⅰ)反应的离子方程式______.
②步骤(Ⅱ)的反应方程式是4Fe(OH)2+2H2O+O2═4Fe(OH)3,制备时应控制“一定量空气”的目的是______.
③由沉淀M获得Fe3O4的过程中发生的反应为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如表:
则X、Y、Z的电负性从大到小的顺序为 (用元素符号表示),元素Y的第一电离能大于X的第一电离能原因是 .
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小.D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取SP3杂化.
①A、B、C的第一电离能由小到大的顺序为 (用元素符号表示).
②M是含有 键的 分子(填“极性”或“非极性”)
③N是一种易液化的气体,请简述其易液化的原因 .
④W分子的VSEPR模型的空间构型为 ,W分子的空间构型为 .
⑤AB-离子中和B2分子的π键数目比为 .
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4S1.
①E元素组成的单质的晶体堆积模型为 (填代号)
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②F元素在其化合物中最高化合价为 .
③G2+离子的核外电子排布式为 ,G2+和N分子形成的配离子的结构式为 .
查看习题详情和答案>>
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2754 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小.D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取SP3杂化.
①A、B、C的第一电离能由小到大的顺序为
②M是含有
③N是一种易液化的气体,请简述其易液化的原因
④W分子的VSEPR模型的空间构型为
⑤AB-离子中和B2分子的π键数目比为
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4S1.
①E元素组成的单质的晶体堆积模型为
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②F元素在其化合物中最高化合价为
③G2+离子的核外电子排布式为
现有A、B、C、D、E五种短周期元素,已知他们的原子序数依次增大,元素A的原子只有一个电子层;又知元素A能分别与元素B、C、D形成电子总数相等的化合物分子X、Y、Z,Y有刺激性气味,Z常温下为液态,元素E的单质的水溶液有漂白性.
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是______;
(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)______,1mol C2A4 参加反应转移电子的数目为______,氧化产物的化学式为______;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为______;
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为______.
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是______.
查看习题详情和答案>>
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是______;
(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)______,1mol C2A4 参加反应转移电子的数目为______,氧化产物的化学式为______;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为______;
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为______.
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是______.
现有A、B、C、D、E五种短周期元素,已知他们的原子序数依次增大,元素A的原子只有一个电子层;又知元素A能分别与元素B、C、D形成电子总数相等的化合物分子X、Y、Z,Y有刺激性气味,Z常温下为液态,元素E的单质的水溶液有漂白性.
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是______;
(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)______,1mol C2A4 参加反应转移电子的数目为______,氧化产物的化学式为______;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为______;
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为______.
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是______ 查看习题详情和答案>>
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是______;
(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)______,1mol C2A4 参加反应转移电子的数目为______,氧化产物的化学式为______;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为______;
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为______.
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是______ 查看习题详情和答案>>
A、B、C、D、E为5种短周期元素,且原子序数依次增大.A的原子半径最小;B的电子总数与其最外层电子数之比为3:2;C的最高价氧化物对应水化物与其简单氢化物反应生成一种盐类物质甲.A、E同主族,A、B、C、E都能分别与D形成原子个数比不同的常见化合物.请回答下列问题:
(1)B在周期表中位于第 族,甲的名称是 .
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为 .在微电子工业中,M的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为 .
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分.现取13.0g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6.72L)和一种固体单质,则乙的化学式是 .
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.汽车内燃机工作时引起反应:C2(g)+D2(g)?2CD(g),是导致汽车尾气中含有CD的原因之一.T℃时,向容积为2L的密闭容器中充入10molC2与5molD2,达到平衡后CD的物质的量为2mol,则T℃时该反应的平衡常数K= (计算结果保留两位有效数字).在其他条件不变的情况下,再通入10molC2与5moD2,达到平衡常数时C2的转化率将 (填“增大”、“减小”或“不变”,下同),CD的平衡浓度将 .
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ?mol-1
△H2= .
查看习题详情和答案>>
(1)B在周期表中位于第
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分.现取13.0g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6.72L)和一种固体单质,则乙的化学式是
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.汽车内燃机工作时引起反应:C2(g)+D2(g)?2CD(g),是导致汽车尾气中含有CD的原因之一.T℃时,向容积为2L的密闭容器中充入10molC2与5molD2,达到平衡后CD的物质的量为2mol,则T℃时该反应的平衡常数K=
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ?mol-1
△H2=