网址:http://m.1010jiajiao.com/timu3_id_60188[举报]
B. 溶液中c(Ca2+)增大
C. 溶液的pH不变
D. 溶液中溶质的质量分数增大
Ⅰ探究NaHCO3溶液在不同温度下pH变化的原因
(1)小组同学测得饱和NaHCO3溶液在不同温度下的pH如下:
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却至 50℃ | pH | 8.3 | 8.4 | 8.5 | 8.8 |
①甲同学认为是温度升高促进了HCO3-的水解,溶液pH增大.写出HCO3-水解的离子方程式:
②乙同学认为溶液pH增大的原因还与NaHCO3在水溶液中受热分解产生Na2CO3有关.Na2CO3水解程度
③丙同学为验证甲、乙两同学的观点,进行了如下实验:
实验1:将加热后的溶液冷却至 10℃,测得此时溶液pH大于8.3;
实验2:在加热煮沸后已冷却的溶液中加入足量的试剂X,产生沉淀.
分析上述验证实验,可说明乙同学观点是
实验2中试剂X是
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
Ⅱ配制1.00mol?L-1NaHCO3溶液,测定其分解率
(2)配制1.00mol?L-1NaHCO3溶液100mL.容量瓶上可以看到的标记是
A.温度 B.容量 C.刻度线 D.溶液物质的量浓度
(3)小组同学取室温下已敞口放置一段时间的上述NaHCO3溶液50.00mL,与足量的稀盐酸反应,测定产生CO2的量,设计了如下装置.
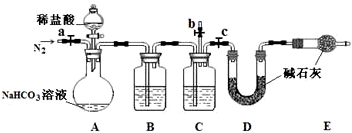
①上述装置C中盛装的试剂为
②往A中加入稀盐酸前,为赶出装置中的空气,先通入N2一段时间.此过程应进行的操作是
③若实验测得D装置增重 2.14g,则溶液中NaHCO3的分解率是
(10分)(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)
A.配制100mL 1.00mol/L的NaCl溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看习题详情和答案>>
(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)
A.配制100mL 1.00mol/L的NaCl 溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3 溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:

①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看习题详情和答案>>(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)
A.配制100mL 1.00mol/L的NaCl 溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3 溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:
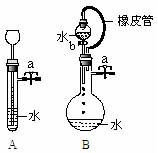 |
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看习题详情和答案>>