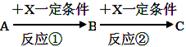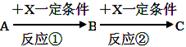摘要:答案:(1)Al C Na2O2 (2)2H2O +Na2O2 =4NaOH+O2↑ 2Al+ 2NaOH+2H2O=2NaAlO2+3H2↑ (3)CO2 CO (4)Na2CO3 (5)2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- [解析]D是淡黄色的固体化合物是本题的突破口.根据中学化学知识基本锁定Na2O2.能与水和CO2反应.但是题目另一信息C是常见的无色无味液体说明C是水.则G为CO2,再依据K能溶于水.说明K为Na2CO3 .F为O2, 题给信息黑色单质B与氧气(F)反应得到G(CO2).说明B为C(碳),依据F(O2)与E反应生成C(水)可知E为氢气.再根据金属A与碱性溶液反应产生氢气.可得到A为Al. [点评]本题框图复杂.纵横交错.难度较大.但是若找到Na2O2这个突破口.本题也就迎刃而解了.
网址:http://m.1010jiajiao.com/timu3_id_59877[举报]
已知A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。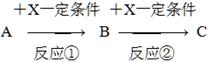
试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为________;C溶液在储存时应加入少量X,理由是(用必要的文字和离子方程式表示)___________________。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________或________。
已知A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
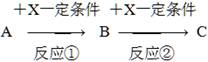
试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为________;C溶液在储存时应加入少量X,理由是(用必要的文字和离子方程式表示)___________________。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________或________。
查看习题详情和答案>>