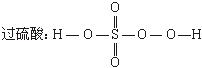
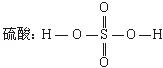摘要:7.答案:②③④. (3)品红溶液褪色,瓶壁有淡黄色粉末和无色的小液滴. (4)SO2+2H2S = 3S↓+2H2O 变大. S H2O. [解析](1)启普发生器制取气体.试剂应选用块状固体和液体.且反应不需要加热.故a.d正确.由于硝酸能氧化-2价硫而得不到H2S.所以b项错. (2)欲控制反应速率.需要控制滴加液体的流速.故要用分液漏斗,若用试管⑤.需要导管.所以用试管④. (3)此问易回答不完整.要先理解反应过程:开始时氧气足量.H2S燃烧生成SO2和H2O,后来氧气不足. 燃烧产物为S和H2O.根据反应过程描述反应现象时.通常要从固.液.气三态来分别考虑其颜色.气 味.光.热等等.以防漏答.此处只要求瓶内的现象.所以可不考虑气味. (5)右部增加的装置为燃烧安全瓶.当安全瓶内燃烧时.乳胶头体积增大.起到减小瓶内压强的作用,这要求安全瓶内的气体与左部反应装置的气体不能相通.所以a错.b对.c.d是排液装置.生成的H2S无法排出.故错误. (6)设空气为100.V(H2S) = 30.V(O2) = 70×= 14.O2不足.所以发生反应2H2S+O22S+2H2O.
网址:http://m.1010jiajiao.com/timu3_id_59772[举报]
常温下,有甲、乙两份体积均为1L,pH均为3的溶液,其中甲为醋酸,乙为盐酸.
①甲用蒸馏水稀释至100倍后,溶液的pH变为a;
②乙与等体积、浓度为1.5mol/L的氨水混合,在此混合液中:n(NH
)+n(H+)-n(OH-)=b mol.
则a、b正确的答案组合是( )
①甲用蒸馏水稀释至100倍后,溶液的pH变为a;
②乙与等体积、浓度为1.5mol/L的氨水混合,在此混合液中:n(NH
+ 4 |
则a、b正确的答案组合是( )
查看习题详情和答案>>
常温下,有甲、乙两份体积均为lL,浓度均为0.1mol/L的氨水,其pH为11.①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2mol/L的盐酸混合,在混合溶液中:n(NH4+)+n(H+)-n(OH-)=bmol.则a、b正确的答案组合是( )
查看习题详情和答案>>
常温下,有甲、乙两份体积均为lL,浓度均为0.1mol/L的氨水,其pH为11.①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2mol/L的盐酸混合,在混合溶液中:n(NH4+)+n(H+)-n(OH-)=bmol.则a、b正确的答案组合是( )
查看习题详情和答案>>
| A.9~11之间; 0.1 | B.9~11之间; 0.2 |
| C.12~13之间; 0.2 | D.13; 0.1 |