网址:http://m.1010jiajiao.com/timu3_id_59451[举报]
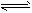 2C(g)达到平衡后,保持其他条件不变,将容器体积扩大到原来的两倍,下列叙述正确的是
2C(g)达到平衡后,保持其他条件不变,将容器体积扩大到原来的两倍,下列叙述正确的是A. 增大 减小 正方向
B. 减小 增大 逆方向
C. 减小 减小 逆方向
D. 增大 增大 正方向
室温下,下列说法正确的是( )
A.将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3
B.HF比HCN易电离,则NaF溶液的pH比同浓度NaCN溶液的pH大
C.向0.1 mol/L氨水中加入少量硫酸铵固体,溶液中 ![]() 增大
增大
D.将1 mL pH=3的HA溶液稀释到10 mL,若溶液的pH<4,则HA为弱酸
查看习题详情和答案>>
新华社2009年10月15日报道:全国农村应当在“绿色生态—美丽多彩—低碳节能—循环发展”的理念引导下,更好更快地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101kPa时:C(s)+![]()
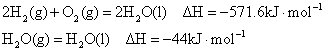
则在25℃,101kPa时:C(s)+H2O(g)=CO(g)+H2(g)△H= 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g) ![]() Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K的值 (填“增大”、“减小”或“不变”)
②1100℃时测得高炉中,c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,则在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是
。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)△H=—49.0kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g)△H=—49.0kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
|
①从反应开始到平衡,氢气的平均反应速率v(H2)= ;
②下列措施能使![]() 增大的是 (填符号)。
增大的是 (填符号)。
A.升高温度 B.再充入H2
C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
查看习题详情和答案>>甲醇是一种非常好的燃料。熔点-97.8°C,沸点64.5°C。一定条件下,
CO与H2反应可制得甲醇:CO+2H2 CH3OH
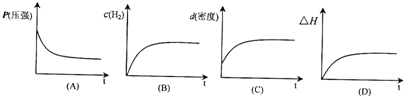
图1表示该反应进行过程中的能量变化:
图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,结合图1写出液态CH3OH燃烧热的热化学方程式 。
(2)根据上图2计算:该温度下,反应CO(g)+2H(g) ![]() CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
A.降低温度 B.加催化剂
C.充入氩气,使体系压强增大 D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压
(3)已知:CH3OH可以在一定条件下转化为HCOOH,HCOOH和CH3COOH性质相似。25°C,0.1mol/LHCOOH溶液的pH>1。室温下,向0.1mol/L的HCOOH溶液中滴加NaOH溶液,当溶液中离子浓度关系满足:
c(HCOO-)<c(Na+)时,则反应的情况可能为 。(填字母)
A.NaOH不足,HCOOH剩余
B.HCOOH与NaOH恰好完全反应
C.NaOH过量
查看习题详情和答案>>
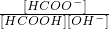 与稀释前比较______(填字母)
与稀释前比较______(填字母)