摘要:30.⑴①2H+ + 2e - = H2↑ 放出气体.溶液变红. ②2Cl - - 2e - = Cl2 ↑ 把湿润的碘化钾淀粉试纸放在Y电极附近.试纸变蓝色. ⑵①纯铜 Cu2+ + 2e - = Cu ②粗铜Cu - 2e - = Cu2+ (3)①4OH--4e-=O2↑+2H2O . ②2H+ + 2e - = H2↑使H+浓度减小③B 2010年高考化学第二轮复习20分钟专题突破(25) 专题 无机推断题
网址:http://m.1010jiajiao.com/timu3_id_57769[举报]
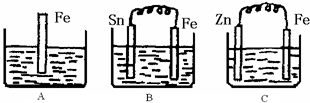 A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸:
A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸:(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
;BFe-2e-=Fe2+
Fe-2e-=Fe2+
; C2H++2e-=H2↑
2H++2e-=H2↑
.(2)一段时间后,B中Sn(锡)极附近溶液的pH
增大
增大
(填“增大”、“减小”、“不变”).(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度为
0.75
0.75
mol?L-1.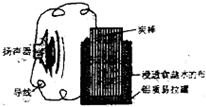 某同学利用家中废旧材料制作一个可使玩具扬声器发出声音的电池,装置如图所示.下列说法正确的是( )
某同学利用家中废旧材料制作一个可使玩具扬声器发出声音的电池,装置如图所示.下列说法正确的是( )