摘要:粉末状试样A是一种含有少量某钾盐和一种活泼金属组成的混合物.进行如下实验: ①将A和适量CuO粉末混合均匀.放在一置于三角架的石棉网上.用酒精灯加强热.可看到混合物迅猛燃烧.白光耀眼.完全反应后得到混合物B. ②向冷却的混合物B中加入稀盐酸至沉淀不再溶解.恰好用去HCl 0.6mol.得到溶液C和沉淀D.然后过滤. ③将溶液C加强热.蒸干.灼烧.得到固体E.且E的质量和A的质量恰好相等. ④如果向溶液C中逐滴加入NaOH溶液.则会出现白色沉淀且逐渐增多.继续滴加NaOH溶液白色沉淀又会逐渐减少.最后完全消失. 请填空: (1)写出①中可能的三个反应的化学方程式 , , . (2)A中金属的质量为 ,所含钾盐的物质的量为 . (3)写出④中先后反应的离子方程式 . .
网址:http://m.1010jiajiao.com/timu3_id_57619[举报]
 已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:
2F2+2H2O=4HF+O2
2F2+2H2O=4HF+O2
;(2)若B是一种四核含18电子的分子,D是一种气态单质分子,则A的化学式为
N2H4
N2H4
,B的结构式为H-O-O-H
H-O-O-H
;(3)若A、B均是含2个原子的微粒,其中B中含有10个电子,D中含有l8个电子,则A、B之间发生反应的离子方程式为
HS-+OH-=S2-+H2O
HS-+OH-=S2-+H2O
;(4)若D是一种含有22个电子的分子,则符合如图所示关系的A的物质有
CH3OH、CH3-CH3
CH3OH、CH3-CH3
(写化学式,如果是有机物则写相应的结构简式).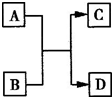 已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:______;
(2)若B是一种四核含18电子的分子,D是一种气态单质分子,则A的化学式为______,B的结构式为______;
(3)若A、B均是含2个原子的微粒,其中B中含有10个电子,D中含有l8个电子,则A、B之间发生反应的离子方程式为______;
(4)若D是一种含有22个电子的分子,则符合如图所示关系的A的物质有______(写化学式,如果是有机物则写相应的结构简式).
查看习题详情和答案>>
(10分)某化学兴趣小组欲研究一种镁铝合金,以下是部分实验。请完成填空。
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol·L—1NaOH溶液(足量)的锥形瓶里。
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体。
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是 。
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据。
| 方法 | 需测定的数据 |
| ① | 测定产生的H2的体积 |
| ② | |
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+。
限选实验用品与试剂:烧杯、试管、滴管、1 mol·L-1NaOH溶液、1 mol·L-1HCl溶液、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。(可填满、可不填满)
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| …… | |
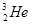 。关于
。关于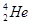 互为同位素
D. 比
互为同位素
D. 比