摘要:3.下列化学实验事实及其解释都正确的是 A.升高温度化学反应速率加快.是因为单位体积内活化分子百分数增加 B.将SO2通入BaCl2溶液.有白色沉淀生成.说明BaSO3难溶于盐酸 C.鸡蛋清溶液中加入饱和CuSO4溶液析出沉淀.说明蛋白质发生了盐析 D.滴有酚酞的Na2CO3溶液中滴加BaCl2溶液后红色变浅.说明BaCl2溶液有酸性 4在一定温度下.恒容密闭容器中.充入一定量的NO和O2.发生2NO+ O22NO2. 反应达到平衡的标志是( ) ①. NO.O2.NO2分子数目比是2:1:2 . ②反应混合物中各组分物质的浓度相等 ③. 混合气体的颜色不再变化 ④. 混合气体的密度不再改变 ⑤混合气体的平均相对分子质量不再变化 ⑥ 2 v O2(正)= V NO2(逆) A ② B ①② C ②③④ D ③ ⑤⑥ 5一定条件下.充分燃烧一定量的丁烷放出热量161.9 kJ.经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液100mL.恰好生成正盐.则此条件下热化学方程式: 的ΔH为 A.+2590.4KJ/mol B. -2590.4KJ/mol C. +1295.2KJ/mol D. -1295.2KJ/mol 6设阿伏加德罗常数的值为NA.则下列说法正确的是 A.常温常压下.18.0 g NH4+中所含的质子数为10 NA B.室温下.8g甲烷含有共价键数为2NA C.111gCaCl2晶体中所含共用电子对的数目为2NA D.常温下.2.7g铝片投入足量的浓硫酸中.铝失去的电子数为0.3NA
网址:http://m.1010jiajiao.com/timu3_id_57594[举报]
下列化学实验事实及其解释都正确的是
A.升高温度化学反应速率加快,是因为单位体积内活化分子百分数增加
B.将SO2通入Ba(NO3)2溶液,有白色沉淀生成,说明BaSO3难溶于硝酸
C.由“同温度下等浓度的Na2CO3溶液比Na2SO3溶液的pH大,可知C比S非金属性弱
D.滴有酚酞的Na2CO3溶液中滴加BaCl2溶液后红色变浅,说明BaCl2溶液有酸性
查看习题详情和答案>>下列化学实验事实及解释都正确的是
A.用滴有少量硫酸铜溶液的稀硫酸跟锌粒反应快速地制氢气,说明Cu2+具有催化能力
B.等体积、![]() 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:
都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:![]()
C.升高温度会加快化学反应速率,其原因是增加了单位体积内活化分子的百分数
D.向浓度均为0.1![]() 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。
的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。
查看习题详情和答案>>
下列化学实验事实及解释都正确的是
A.用滴有少量硫酸铜溶液的稀硫酸跟锌粒反应快速地制氢气,说明Cu2+具有催化能力
B.等体积、![]() 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:
都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:![]()
C.升高温度会加快化学反应速率,其原因是增加了单位体积内活化分子的百分数
D.向浓度均为0.1![]() 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。
的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。
查看习题详情和答案>>
 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:
都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:
 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明
的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明
 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:
都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性: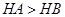
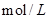 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。
的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]。