摘要:1.某温度下.在100g水中加入一定质量的无水硫酸铜.或加入一定质量的硫酸铜晶体.完全溶解后所得溶液的溶质质量分数相等.则所加两种物质的质量关系为 .
网址:http://m.1010jiajiao.com/timu3_id_5756[举报]
在一定温度下,某无水盐R在水中溶解度为23g,向R的饱和溶液中加入Bg该无水盐,保持温度不变,析出R的结晶水合物Wg,从原饱和溶液中析出溶质R的质量为
A.23(W-B)/123g B.23(W-B)/77g
C.23(W-B)/100g D.(W-77B/23)/g
查看习题详情和答案>>在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液可采取的方法有:①升高温度,②降低温度,③增加硝酸钾,④减少硝酸钾,⑤增加溶剂,⑥减少溶剂.其中正确的一组是
[ ]
A.①②③
B.②③④
C.③④⑤
D.②③⑥
(1)一变:某温度时的硝酸钾饱和溶液,加盖密封,当温度变化时,溶液是
[ ]
A.变成不饱和溶液或析出晶体
B.变成不饱和溶液
C.析出晶体后变成不饱和溶液
D.仍为饱和溶液
(2)二变:在mg硝酸钾饱和溶液中,加入ng销酸钾晶体(保持温度不变),则单位质量溶液中,硝酸钾的质量
[ ]
A.增大
B.不变
C.减小
D.无法判断
(3)三变:20℃硝酸钾饱和溶液100g,蒸发掉20g水后恢复到20℃,则溶液中保持不变的是
[ ]
A.溶液质量
B.溶剂质量
C.溶解度
D.溶质质量
在一定温度下向100g溶质质量分数为a%的某物质的水溶液中,加入w g该物质至完全溶解,恰好达到饱和,则此温度下该物质的溶解度为________,该饱和溶液中溶质的质量分数为________.
查看习题详情和答案>>下列说法正确的是
- A.在相同温度下同一溶质的饱和溶液一定比与不饱和溶液所含溶质的质量多
- B.在20℃时,将KNO3溶液蒸发5g水析出ag晶体,再蒸发5g水又析出bg晶体,则a≤b
- C.若将50g浓度为10%的NaCl溶液浓度增大一倍,可以再加入5gNaCl晶体
- D.已知某K2CO3和KOH的混合溶液中,加入100g浓度为9.8%稀硫酸恰好完全反应,反应后所得溶液中溶质的质量一定为17.4g
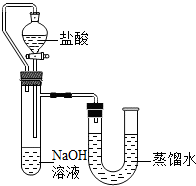 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.(1)配制100g质量分数为8%的氢氧化钠溶液.
①计算:需要氢氧化钠固体的质量为
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温.
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签.
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
①用pH试纸测定NaOH溶液pH时,正确的操作是:
②简述强调“测得的pH小于7”的理由:
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.该组同学在没使用温度计的情况下,通过如图所示装置完成了实验.则该组同学根据