摘要:24. 减少SO2的排放.回收利用SO2是环保的重要课题.我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2.制备硫酸锰的生产流程如下: 浸出液的pH<2.其中的金属离子主要是Mn2+.还含有少量的Fe2+.Al3+.Ca2+.Pb2+等其它金属离子. 有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表.阳离子吸附剂吸附金属离子 的效果见下图. 离子 离子半径(pm) 开始沉淀时的pH 完全沉淀时的pH Fe2+ 74 7.6 9.7 Fe3+ 64 2.7 3.7 Al3+ 50 3.8 4.7 Mn2+ 80 8.3 9.8 Pb2+ 121 8.0 8.8 Ca2+ 99 - - 已知PbO2的氧化性强于MnO2.请回答下列问题: ⑴ 写出浸出过程中主要反应的化学方程式 . 氧化过程中主要反应的离子方程式 . ⑵ 在氧化后的液体中加入石灰浆.用于调节pH.pH应调节至范围 . 滤渣的主要成分有 . ⑶ 阳离子吸附剂用于除去杂质金属离子.决定阳离子吸附剂吸附效果的因素是 . a.溶液的pH b.金属离子的氧化性 c.金属离子的半径 d.吸附时间 ⑷ 操作a包括 过程.
网址:http://m.1010jiajiao.com/timu3_id_56041[举报]
减少SO2的排放、回收利用SO2是环保的重要课题。我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2,制备硫酸锰的生产流程如下:

浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其它金属离子。
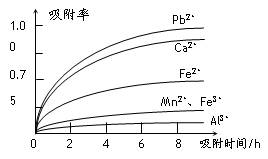
有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
已知PbO2的氧化性强于MnO2。请回答下列问题:
⑴ 写出浸出过程中主要反应的化学方程式 ,
氧化过程中主要反应的离子方程式 。
⑵ 在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至范围 ,
滤渣的主要成分有 。
⑶ 阳离子吸附剂用于除去杂质金属离子。决定阳离子吸附剂吸附效果的因素是
(填写序号)。
a.溶液的pH b.金属离子的氧化性 c.金属离子的半径 d.吸附时间
⑷ 操作a包括 过程。
查看习题详情和答案>>
保护自然环境已成为人类社会可持续发展的重要课题.
(1)正常雨水偏酸性,pH约为 (填“5.6”、“7.0”或“8.4”),这是因为大气中的CO2溶于雨水生成了碳酸,该反应的化学方程式为 .某工厂每小时燃烧含硫1%的煤5t,若硫全部转化为SO2,则该厂每天产生SO2 t.下列反应可减少SO2的排放量:2CaCO3+O2+2SO2═2X+2CO2,其中X的化学式为 .
(2)用硫酸处理含烧碱废水的有关反应的离子方程式为 .
(3)下列做法不利于节能减排、保护环境的是 (填字母代号).
A.推广使用无磷洗涤剂 B.开发利用太阳能、风能、地热能等
C.推广垃圾分类、回收利用 D.大量使用一次性筷子和塑料袋等. 查看习题详情和答案>>
(1)正常雨水偏酸性,pH约为
(2)用硫酸处理含烧碱废水的有关反应的离子方程式为
(3)下列做法不利于节能减排、保护环境的是
A.推广使用无磷洗涤剂 B.开发利用太阳能、风能、地热能等
C.推广垃圾分类、回收利用 D.大量使用一次性筷子和塑料袋等. 查看习题详情和答案>>