网址:http://m.1010jiajiao.com/timu3_id_54225[举报]
(09盐城第三次调研)在Ni、NiO、Ni3C、γ-Al2O3组成的催化剂表面,可实现H2O、CO2及CH4合成乙醇。
 (1)下列说法正确的是 (选填序号)。
(1)下列说法正确的是 (选填序号)。
A.第一电离能:碳原子大于氧原子
B.CO2分子中含有2个σ键和2个π键
C.CH4分子中碳原子采用sp3杂化
D.二甲醚的沸点比乙醇高
(2)镍原子基态时的核外电子排布式 。
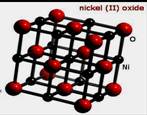
(3)NiO晶胞如右上图所示,每个晶胞中与每个Ni2+距离相等且最近的Ni2+有 个,某种有缺陷的氧化镍晶体
由Ni2+、Ni3+、O2-及空隙组成,可表示为Ni0.98O,则n(Ni2+)/n(Ni3+)= 。
(4)对苯二甲酸( ![]() )、4,4’-联吡啶[
)、4,4’-联吡啶[![]() (可简化为
(可简化为 ![]() )]等与Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如下图:
)]等与Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如下图:

该络合物中配位原子是: ;依据价层互斥理论,ClO4-空间结构为 型。
查看习题详情和答案>>(09盐城第三次调研)一些较活泼的金属在某些特定的介质环境中,会变为惰性状态,这是由于金属表面上覆盖了一层氧化膜。铁在不同浓度的硝酸中溶解与钝化情况如图如示。试探究下列问题:
(1)现有一枚光亮的铁钉,欲使其表面形成钝化层,应将其放入浓度大于 的硝酸中一段时间;证明其表面已形成一层致密的钝化层的简单实验是: 。
(2)下列有关说法不正确的是 (选填序号)。
![]()
A.铜难溶于冷的浓硫酸,是因为铜在浓硫酸中发生钝化
B.铜片和铝片用导线连接后插入冷的浓硝酸中,电流一定总是由铜电极沿导线流入铝极
C.铁在硝酸溶液中的腐蚀速率与硝酸浓度一定呈正比
D.可用冷的浓硝酸除去铝制容器内的水垢
(3)发蓝液是由NaNO3、NaNO2及NaOH配成的,在加热条件下,通过三步反应使铁表面生成一层致密的Fe3O4:3Fe+NaNO2+5NaOH![]() 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①;
8Fe+3NaNO3+5NaOH+2H2O![]() 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;
以及第三步生成四氧化三铁。请补充第三步反应的方程式并配平: 。
(4)为了使铝表面形成较厚的氧化膜,工业上常用电解硫酸溶液的方法,在阳极上生成氧化铝,写出此时阳极的电极反应: 。
查看习题详情和答案>>(08浙江严州中学三模)臭氧是氧气吸收了太阳的波长小于185nm的紫外线后形成的,不过当波长在25nm左右的紫外线照射臭氧时,又会使其生成氧气。下列说法中正确的是( )
A. 臭氧有漂白作用,其漂白原理与SO2的漂白原理相同
B. 臭氧转化为氧气和氧气转化为臭氧均需要吸收能量
C. 和氧气比较,臭氧的氧化性较强,臭氧的能量较高
D. 臭氧和氧气互为同素异形体,它们之间的转化是物理变化
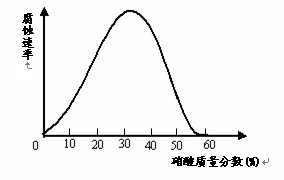
查看习题详情和答案>>(10分)TBC是优良的增塑剂,具有很好的相容性,且挥发性小、耐寒、耐光及耐水等,广泛用于医学卫生用品,它的结构式如下图,合成时柠檬酸与正丁醇合成数据如下:

下表中实验数据均为用活性炭固体杂多酸作催化剂,实验时催化剂总量占原料的1%,实验结果如下表。表1:酸醇物质的量之比对酯化率的影响;表2:酯化时间对酯化率的影响;表3:酯化率随温度变化情况。
表1 | n(酸)n(醇) | 15.0 | 15.5 | 16.0 | 16.5 | 17.0 |
酯化率/% | 95.1 | 96.3 | 97.0 | 97.4 | 97.2 | |
表2 | 时间/h | 0.5 | 1.0 | 2.0 | 3.0 | 5.0 |
酯化率/% | 40.0 | 70.2 | 94.3 | 97.4 | 97.4 | |
表3 | 温度/℃ | 130 | 140 | 145 | 150 | 160 |
酯化率/% | 89.5 | 96.2 | 97.4 | 97.4 | 97.2 |
试回答下列问题
(1)酯化反应适宜的条件n(酸)∶(醇)、时间/h、温度/℃分别是: (选填序号)。
 A.1∶5,1,130 B.1∶5.5 ,1,140
A.1∶5,1,130 B.1∶5.5 ,1,140
C.1∶7 ,2,160 D.1∶6.5 ,3,145
(2)温度太高酯化率降低的可能原因是
(3)TBC的一种标准谱图如右,它是
(A、1H-NMR图谱 B、红外光谱 C、质谱)
(4)TBC与足量NaOH溶液反应的化学方程式: 。(5)柠檬酸的一种同分异构体A,能发生如下转化:
A可能的结构式为: (只写一种)。
查看习题详情和答案>>