摘要:14.一定质量的Fe2O3.ZnO.CuO的固体混合粉末.在加热条件下用足量CO还原.得到金属混合物4.82g.将生成的CO2气体用足量的澄清石灰水吸收后.产生l0g白色沉淀.若用2mol·L-1的盐酸溶解该混合物.至少需要盐酸的体积为 A.50 mL B.100 mL C.200 mL D.缺少数据.无法计算
网址:http://m.1010jiajiao.com/timu3_id_53944[举报]
(2012?吉林一模)为测定FeO和Fe2O3固体混合物中Fe元素的含量,可用氢气还原一定质量的此混合物并测定生成水的质量的方法来完成.若在实验室中选用下列实验装置来实现上述目的(图中夹持装置已略去,部分装置可重复使用).请填空:

(1)仪器X的名称是
(2)装置A中发生反应的离子方程式为
(3)装置B中发生反应的化学方程式为
(4)图①-④示装置中与A装置具有相同作用的是
(5)按正确的实验设计,所连接的装置顺序为:A→C→
(6)若FeO和Fe2O3混合物的质量为ag,反应完全后生成水的质量为bg,则混合物中Fe元素的质量分数为
×100%
×100%(用含字母的数学式表示).
查看习题详情和答案>>

(1)仪器X的名称是
长颈漏斗
长颈漏斗
.(2)装置A中发生反应的离子方程式为
Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
,实验前检验装置A的气密性的方法是关闭活塞K,向长颈漏斗中加水至其液面高于试管中的液面,(停止加水)一段时间后液面高度差没变化,说明装置不漏气
关闭活塞K,向长颈漏斗中加水至其液面高于试管中的液面,(停止加水)一段时间后液面高度差没变化,说明装置不漏气
.(3)装置B中发生反应的化学方程式为
FeO+H2
Fe+H2O或Fe2O3+3H2
2Fe+3H2O
| ||
| ||
FeO+H2
Fe+H2O或Fe2O3+3H2
2Fe+3H2O
(任写一个即可).
| ||
| ||
(4)图①-④示装置中与A装置具有相同作用的是
①④
①④
(填装置编号).(5)按正确的实验设计,所连接的装置顺序为:A→C→
B
B
→C
C
→C
C
.(6)若FeO和Fe2O3混合物的质量为ag,反应完全后生成水的质量为bg,则混合物中Fe元素的质量分数为
| 1-8b |
| 9a |
| 1-8b |
| 9a |
(2013?临沂一模)工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知:Cu2O+2H+═Cu+Cu2++H2O
(1)实验操作I的名称为
(2)滤液A中铁元素的存在形式为
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=
(5)①利用电解法进行粗铜精炼时,下列叙述正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
②从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→
查看习题详情和答案>>

已知:Cu2O+2H+═Cu+Cu2++H2O
(1)实验操作I的名称为
过滤
过滤
;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有坩埚
坩埚
(填仪器名称).(2)滤液A中铁元素的存在形式为
Fe2+
Fe2+
(填离子符号),生成该离子的离子方程式为2Fe3++Cu═2Fe2++Cu2+
2Fe3++Cu═2Fe2++Cu2+
,检验滤液A中存在该离子的试剂为KSCN溶液
KSCN溶液
(填试剂名称).(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为
2 Al+Fe2O3
Al2O3+2Fe
| ||
2 Al+Fe2O3
Al2O3+2Fe
.
| ||
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=
11
11
.(5)①利用电解法进行粗铜精炼时,下列叙述正确的是
b.c
b.c
(填代号).a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
②从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→
将浓硫酸用蒸馏水稀释,将样品与稀硫酸充分反应后
将浓硫酸用蒸馏水稀释,将样品与稀硫酸充分反应后
→过滤、洗涤、干燥→称量剩余固体铜的质量.(填缺少的操作步骤,不必描述操作过程的细节)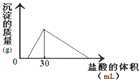 (1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
(1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).NO3-+
10Al
10Al
+18H2O
18H2O
→10Al(OH)3
10Al(OH)3
+3N2
3N2
+6OH-
6OH-
该反应过程中,被氧化与被还原的元素的物质的量之比为5:3
5:3
.(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol
Fe2O3(s)+
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)=CO2(g)△H=-c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
| 1 |
| 2 |
| 3 |
| 2 |
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
.| 1 |
| 2 |
| 3 |
| 2 |
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为
2.016
2.016
L(标准状况).
Fe2O3具有广泛的用途.
甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3.为了进一步验证此结论,他做了如下实验:
由此甲同学得出结论:4FeCO3+O2
2Fe2O3+4CO2
(1)写出实验步骤Ⅲ中发生反应的离子方程式 .
(2)乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+.于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+.他需要选择的试剂是 (填序号).
a.氯水 b.氯水+KSCN溶液 c.K3[Fe(CN)6](铁氰化钾溶液)
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分.你认为丙同学持此看法的理由是 .
(4)丙同学进一步查阅资料得知,煅烧FeCO3的产物中,的确含有+2价铁元素.于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、 (填名称)和 (填名称);再 (填操作名称),灼烧,即可得到Fe2O3.
查看习题详情和答案>>
甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3.为了进一步验证此结论,他做了如下实验:
| 实验步骤 | 实验操作 |
| I | 取一定质量的FeCO3固体置于坩埚中,高温燃烧至质量不再减轻,冷却至室温. |
| II | 取少量实验步骤I所得固体放于一洁净的试管中,用足量的稀硫酸溶解. |
| III | 向实验步骤II所得溶液中滴加KSCN溶液,溶液变红. |
| ||
(1)写出实验步骤Ⅲ中发生反应的离子方程式
(2)乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+.于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+.他需要选择的试剂是
a.氯水 b.氯水+KSCN溶液 c.K3[Fe(CN)6](铁氰化钾溶液)
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分.你认为丙同学持此看法的理由是
(4)丙同学进一步查阅资料得知,煅烧FeCO3的产物中,的确含有+2价铁元素.于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、