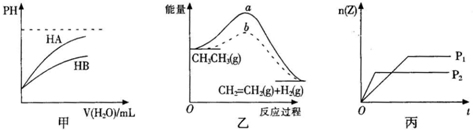
摘要:6.反应aX cZ(g),∆H<0.在不同温度(T1和T2)及压强(P1和P2)下.产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是:( ) A.T1<T2.P1<P2,a+b<c B.T1<T2.P1>P2, a+b<c C.T1>T2.P1>P2, a+b>c D.T1>T2.P1<P2 ,a+b>c
网址:http://m.1010jiajiao.com/timu3_id_51173[举报]
对于可逆反应aX+bY?cZ+dw中,a、b、c、d为系数,下面5个图均为处于平衡状态时各混合气体中Z%随温度,压强变化的曲线:
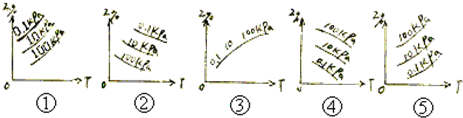
从图中选出是下列反应相对应的曲线,用序号填空
(1)正反应属于放热反应的是
(2)逆反应属于放热反应的是
(3)化学计量数符合a+b>c+d的是
(4)化学计量数符合a+b<c+d的是
(5)图③反应出化学计量数的关系是
查看习题详情和答案>>

从图中选出是下列反应相对应的曲线,用序号填空
(1)正反应属于放热反应的是
②④
②④
(2)逆反应属于放热反应的是
①③⑤
①③⑤
(3)化学计量数符合a+b>c+d的是
④⑤
④⑤
(4)化学计量数符合a+b<c+d的是
①②
①②
(5)图③反应出化学计量数的关系是
a+b=c+d
a+b=c+d
(填数学式)恒温下,反应aX(g)?bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1mol/L增大到0.19mol/L,下列判断正确的是( )
查看习题详情和答案>>
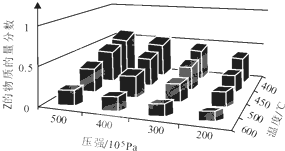 为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如右图所示.以下判断正确的是( )
为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如右图所示.以下判断正确的是( )| A、△H>0,a+b>c | B、△H>0,a+b<c | C、△H<0,a+b>c | D、△H<0,a+b<c |
 bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍.则下列叙述正确的是( )
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍.则下列叙述正确的是( )