摘要:28.已知将浓盐酸滴入高锰酸钾溶液中.产生黄绿色气体.而溶液的紫红色褪去.现有一氧化还原反应的体系中.共有KCl.Cl2.浓H2SO4.H2O.KMnO4.MnSO4.K2SO4七种物质: (1)该氧化还原反应的体系中.还原剂是 .化合价没有发生变化的反应物是 . (2)写出一个包含上述七种物质的氧化还原反应方程式: . (3)上述反应中.1 mol氧化剂在反应中转移的电子为 mol. (4)如果在反应后的溶液中加入NaBiO3.溶液又变为紫红色.BiO3-反应后变为无色的Bi3+.证明NaBiO3的一个性质是: .
网址:http://m.1010jiajiao.com/timu3_id_49769[举报]
 已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质.
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质.(1)该反应中,化合价升高的反应物是
KCl
KCl
.(2)写出一个包含上述七种物质的氧化还原反应方程式:
2KMnO4+10KCl+8H2SO4═2MnSO4+6K2SO4+5Cl2↑+8H2O
2KMnO4+10KCl+8H2SO4═2MnSO4+6K2SO4+5Cl2↑+8H2O
.(3)上述反应中,1mol氧化剂在反应中得到
5
5
mol电子.(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C
安全作用防止D中液体倒吸入集气管B装置中
安全作用防止D中液体倒吸入集气管B装置中
;D尾气吸收,防止有毒气体氯气扩散到空气中污染空气
尾气吸收,防止有毒气体氯气扩散到空气中污染空气
.(5)某浓盐酸的密度l.198g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=40%.则质量分数W2=20%的盐酸其物质的量浓度C2
小于
小于
(填大于、等于或小于)6.565mol?L-1. 已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质.
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质.
(1)该反应中,化合价升高的反应物是______.
(2)写出一个包含上述七种物质的氧化还原反应方程式:______.
(3)上述反应中,1mol氧化剂在反应中得到______mol电子.
(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C______;D______.
(5)某浓盐酸的密度1.198g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=40%.则质量分数W2=20%的盐酸其物质的量浓度C2______(填大于、等于或小于)6.565mol?L-1.
查看习题详情和答案>>
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有3Cl、Cl2、H2SO4、H2O、3MnO4、MnSO4、32SO4七种物质.
(1)该反应中,化合价升高的反应物是______.
(2)写出一个包含上述七种物质的氧化还原反应方程式:______.
(3)上述反应中,1mol氧化剂在反应中得到______mol电子.
(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C______;D______.
(多)某浓盐酸的密度l.1d8g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=4中%.则质量分数W2=2中%的盐酸其物质的量浓度C2______(填大于、等于或小于)6.多6多mol?L-1.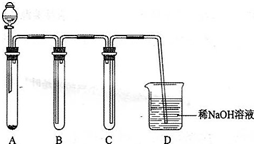
查看习题详情和答案>>
(1)该反应中,化合价升高的反应物是______.
(2)写出一个包含上述七种物质的氧化还原反应方程式:______.
(3)上述反应中,1mol氧化剂在反应中得到______mol电子.
(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C______;D______.
(多)某浓盐酸的密度l.1d8g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=4中%.则质量分数W2=2中%的盐酸其物质的量浓度C2______(填大于、等于或小于)6.多6多mol?L-1.

已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl.Cl2.H2SO4.H2O.KMnO4.MnSO4.K2SO4七种物质:
(1)该反应中,化合价升高的反应物是 。
(2)写出一个包含上述七种物质的氧化还原反应方程式:
(3)上述反应中,氧化剂是 ,1 mol氧化剂在反应中得到 mol电子。
(4)将某密度为l.19g·cm-3,质量分数为36.5%的浓盐酸,配制成500mL0.5mol/L的稀盐酸,所需浓盐酸的体积为 。
查看习题详情和答案>>
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质.
(1)该反应中,化合价升高的反应物是______.
(2)写出一个包含上述七种物质的氧化还原反应方程式:______.
(3)上述反应中,1mol氧化剂在反应中得到______mol电子.
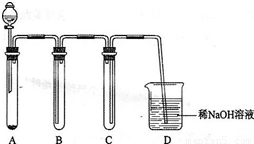
(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C______;D______.
(5)某浓盐酸的密度l.198g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=40%.则质量分数W2=20%的盐酸其物质的量浓度C2______(填大于、等于或小于)6.565mol?L-1.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)该反应中,化合价升高的反应物是______.
(2)写出一个包含上述七种物质的氧化还原反应方程式:______.
(3)上述反应中,1mol氧化剂在反应中得到______mol电子.
(4)如图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答下列有关问题:装置C、D的作用分别是:C______;D______.
(5)某浓盐酸的密度l.198g?cm-3,该盐酸的物质的量浓度C1=13.13mol?L-1,溶质HCl的质量分数为W1=40%.则质量分数W2=20%的盐酸其物质的量浓度C2______(填大于、等于或小于)6.565mol?L-1.
 查看习题详情和答案>>
查看习题详情和答案>>