摘要:37.①KBrO3>KIO3>Br2>I2 ②1∶6 ③10I-+2BrO3-+12H+ 5I2+Br2+6H2O ④I2.KIO3.Br2
网址:http://m.1010jiajiao.com/timu3_id_49668[举报]
已知酸性条件下有以下反应关系:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2。
②Br2能将I-氧化为I2。
③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2。
(1)氧化剂(Br2、KBrO3、KIO3)氧化能力由强到弱的顺序为____。
(2)现向含有1 mol KI的硫酸溶液中加入含amol KBrO3的溶液,a的取值不同,所得产物也不同。试将讨论的结果填入下表中:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2。
②Br2能将I-氧化为I2。
③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2。
(1)氧化剂(Br2、KBrO3、KIO3)氧化能力由强到弱的顺序为____。
(2)现向含有1 mol KI的硫酸溶液中加入含amol KBrO3的溶液,a的取值不同,所得产物也不同。试将讨论的结果填入下表中:
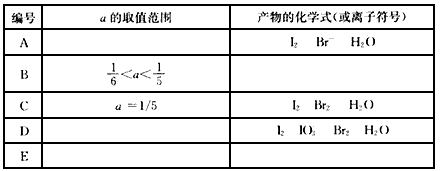
(3)若产物中碘单质和溴单质的物质的量相等时,a的值为____。
查看习题详情和答案>>
已知在酸性条件下有如下关系:
①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2;
②Br2能把I-氧化成I2;
③KIO3能把I-氧化成I2;
④KIO3能把Br-氧化成Br2。在③、④反应中KIO3被还原为I2。
试回答下列问题:
(1) KBrO3、KIO3、Br2、I2的氧化性由弱到强的顺序为_______________________。
(2)现取6L 0.4mol·L-1 KBrO3溶液和10L 0.4mol·L-1 KI溶液在稀H2SO4中混合发生反应,所得氧化产物为
________ (填化学式),其物质的量为________。
查看习题详情和答案>>
①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2;
②Br2能把I-氧化成I2;
③KIO3能把I-氧化成I2;
④KIO3能把Br-氧化成Br2。在③、④反应中KIO3被还原为I2。
试回答下列问题:
(1) KBrO3、KIO3、Br2、I2的氧化性由弱到强的顺序为_______________________。
(2)现取6L 0.4mol·L-1 KBrO3溶液和10L 0.4mol·L-1 KI溶液在稀H2SO4中混合发生反应,所得氧化产物为
________ (填化学式),其物质的量为________。
已知在酸性条件下有如下关系:①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2;②Br2能氧化I-为I2③KIO3能氧化I-为I2;④KIO3能氧化Br-为 Br2。在③④反应中KlO3被还原为I2。试回答:
(1)KBrO3、KIO3、Br2、I2氧化性由弱到强的顺序。
(2)现取6mL0.4mo1·L-1KBrO3溶液和10mL0.4mo1·L-1KI溶液在稀H2SO4中混合,
生成的产物是什么?物质的量之比为多少?
查看习题详情和答案>>
已知在酸性条件下有如下关系:①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2;②Br2能氧化I-为I2③KIO3能氧化I-为I2;④KIO3能氧化Br-为 Br2。在③④反应中KlO3被还原为I2。试回答:
(1)KBrO3、KIO3、Br2、I2氧化性由弱到强的顺序。
(2)现取6mL0.4mo1·L-1KBrO3溶液和10mL0.4mo1·L-1KI溶液在稀H2SO4中混合,
生成的产物是什么?物质的量之比为多少?
查看习题详情和答案>>
(2008?闵行区模拟)在酸性条件下:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原成Br2;
②KIO3能将I-氧化为I2,也能将Br-氧化成Br2,其本身被还原成I2.
(1)上述反应所涉及到的粒子氧化性最强的是
(2)写出一个能证明氧化性Br2>I2的离子方程式
(3)向含有KI、H2SO4的溶液中加入KBrO3溶液,若氧化产物、还原产物只有I2和Br2,写出反应的化学方程式,并标明电子转移方向和数目.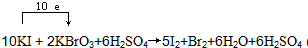
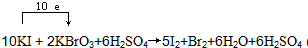 ;其中被氧化的元素是
;其中被氧化的元素是
查看习题详情和答案>>
①KBrO3能将KI氧化成I2或KIO3,其本身被还原成Br2;
②KIO3能将I-氧化为I2,也能将Br-氧化成Br2,其本身被还原成I2.
(1)上述反应所涉及到的粒子氧化性最强的是
BrO3-
BrO3-
(填离子符号);(2)写出一个能证明氧化性Br2>I2的离子方程式
Br2+2I-→I 2+2 Br-
Br2+2I-→I 2+2 Br-
;(3)向含有KI、H2SO4的溶液中加入KBrO3溶液,若氧化产物、还原产物只有I2和Br2,写出反应的化学方程式,并标明电子转移方向和数目.
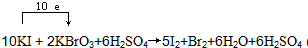
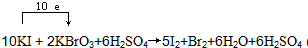
-1价I
-1价I
,要得到1mol还原产物转移电子数目为6.02×1024
6.02×1024
.