摘要: Ⅰ(1)洗去铝表面的油污. A l2O3+2OH-+3H2O=2Al(OH)4-或A l2O3+2OH-=2AlO2-+H2O (2)2 A l +3 H2O-6e = A l2O3+6H+ Ⅱ 排除氢离子浓度不同对反应的影响.探究氯离子和硫酸根离子对反应的影响. 氯离子对氧化铝膜有破坏作用.因此铝制容器不有长期盛放含氯离子的食品.
网址:http://m.1010jiajiao.com/timu3_id_48321[举报]
(2008?茂名二模)生产着色铝片的工艺流程如下:
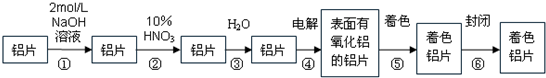
请回答下列问题:
(1)第①步中NaOH溶液的作用是
(2)第②步HNO3的作用是对铝片进行抛光,写出其反应的离子方程式
(3)在第④步电解是以铝为阴极,铝片为阳极,在硫酸介质中控制电压电流,使阳极放出O2与Al反应使铝表面形成一层致密的氧化膜.写出有关的电极反应式:阴极:
(4)氧化膜质量的检验:取出铝片干燥,在氧化膜未经处理的铝片上分别滴一滴氧化膜质量检查液(3gK2CrO4+75mL水+25mL浓盐酸),判断氧化膜质量的依据是
A.铝片表面有无光滑 B.比较颜色变化
C.比较质量大小 D.比较反应速率大小
(5)将已着色的铝干燥后在水蒸气中进行封闭处理约20~30min,封闭的目的是使着色的氧化膜更加致密,有关反应化学方程式是
查看习题详情和答案>>

请回答下列问题:
(1)第①步中NaOH溶液的作用是
洗去铝表面的油污
洗去铝表面的油污
.(2)第②步HNO3的作用是对铝片进行抛光,写出其反应的离子方程式
Al+4H++NO3-=Al3++NO↑+2H2O
Al+4H++NO3-=Al3++NO↑+2H2O
.(3)在第④步电解是以铝为阴极,铝片为阳极,在硫酸介质中控制电压电流,使阳极放出O2与Al反应使铝表面形成一层致密的氧化膜.写出有关的电极反应式:阴极:
6H++6e-=H2↑
6H++6e-=H2↑
,阳极:2Al+3H2O-6e-=Al2O3+6H+
2Al+3H2O-6e-=Al2O3+6H+
.(4)氧化膜质量的检验:取出铝片干燥,在氧化膜未经处理的铝片上分别滴一滴氧化膜质量检查液(3gK2CrO4+75mL水+25mL浓盐酸),判断氧化膜质量的依据是
B
B
.A.铝片表面有无光滑 B.比较颜色变化
C.比较质量大小 D.比较反应速率大小
(5)将已着色的铝干燥后在水蒸气中进行封闭处理约20~30min,封闭的目的是使着色的氧化膜更加致密,有关反应化学方程式是
2Al+3H2O(g)
Al2O3+3H2(g)
| ||
2Al+3H2O(g)
Al2O3+3H2(g)
.
| ||
下列有关物质的性质与应用相对应的是
A.炭具有强还原性,常用于冶炼镁、钠等金属
B.铝的金属性较强,可用作飞机、火箭的结构材料
C.碳酸钠溶液呈碱性,可用于洗去铁屑表面的油污
D.浓硫酸具有强氧化性,可用于与亚硫酸钠反应制取二氧化硫
查看习题详情和答案>>